Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista internacional de contaminación ambiental
versión impresa ISSN 0188-4999
Rev. Int. Contam. Ambient vol.30 no.2 Ciudad de México may. 2014
Identificación de zonas de contaminación por nitratos en el agua subterránea de la zona sur de la Cuenca de México
Identification of nitrate pollution zones in groundwater south of the Mexican Basin
Silvia MONTIEL PALMA1, María Aurora ARMIENTA HERNÁNDEZ2*, Ramiro RODRÍGUEZ CASTILLO2 y Eloísa DOMÍNGUEZ MARIANI3
1 Posgrado en Ciencias de la Tierra, Universidad Nacional Autónoma de México
2 Instituto de Geofísica, Universidad Nacional Autónoma de México *Autora responsable; aurora.armienta@gmail.com
3 Universidad Autónoma Metropolitana, Lerma
Recibido enero 2014,
aceptado abril 2014
RESUMEN
El presente trabajo aborda la evaluación de los niveles de nitratos y su comportamiento geoquímico en el agua subterránea de una zona en el sur de la Cuenca de México. La caracterización hidrogeoquímica se realizó a partir de la información de 42 pozos de abastecimiento por medio de mapas de isoconcentraciones, diagramas de Piper, secciones geológicas, así como el análisis del comportamiento de los iones NO3-, SO42-, Cl-, HCO3, Ca2+, Mg2+, Na+ y conductividad eléctrica a lo largo del flujo en el acuífero somero. El área de estudio está compuesta principalmente de rocas volcánicas fracturadas en las estribaciones de las Sierras del Ajusco y Chichinautzin al oeste y depósitos lacustres y arcillas al este. La interpretación geoquímica del agua muestra una dirección de flujo radial desde las sierras hacia la zona lacustre. Las concentraciones de nitratos fueron inferiores a los límites establecidos para agua potable excepto en uno de los pozos. Las áreas con mayores contenidos de nitratos determinadas en este trabajo se ubican hacia el oeste en las faldas de la Sierra Chichinautzin y en las inmediaciones del Periférico Sur en Tepepan. La distribución de concentraciones mostró una tendencia decreciente desde la sierra Chichinautzin hacia la zona lacustre proviniendo de la zona de recarga del acuífero. Las secciones geológicas mostraron que las concentraciones de sulfatos y la relación NO3-: Cl- decrecen espacialmente en la dirección del flujo subterráneo. Esto sugiere que las condiciones oxidantes del entorno disminuyen de la periferia al centro, hasta llegar al límite con las arcillas lacustres de la planicie. Estas arcillas están localizadas en la parte superior de la columna estratigráfica local del pozo muestreado más alejado de la zona de recarga. Los resultados analíticos de dicho pozo mostraron la presencia de nitritos que reflejan condiciones reductoras.
Palabras clave: Ciudad de México, Sierra Chichinautzin, hidrogeoquímica, nitratos, nitritos.
ABSTRACT
Assessment of drinking groundwater quality south of the Basin of Mexico was carried out using as indicators the concentration of nitrates jointly with geochemical behavior. Hydrogeochemical characterization was based on the composition of 42 supply wells by means of iso-concentration maps, Piper diagrams, geological sections, and the behavior of NO3-, SO42-, Cl-, HCO3-, Ca2+, Mg2+, Na+ and electrical conductivity along groundwater flow in the shallow aquifer. The study area is constituted mostly by fractured volcanic rocks in the lower slopes of Ajusco and Chichinautzin ravines to the west, and lacustrine deposits and clays to the east. Geochemical interpretation showed a radial flow from the ravines to the lacustrine zone. Nitrate concentrations were lower than drinking water standards in all but one well. The areas with highest nitrate concentrations identified in this study, are located to the west in the Chihinautzin ravine slopes and in Tepepan close to Periférico Sur. Concentration distribution showed a decreasing trend from the ravines in the recharge zone, to the lacustrine area. Water chemistry along geological sections showed a decrease of sulfates concentration and NO3-: Cl- ratio along groundwater flow. This suggests that oxidizing conditions decrease from the periphery to the center until reaching the lacustrine clays of the plain. These clays are located in the upper part of the stratigraphic column of the farthest well from the recharge zone in the studied geological section. Analysis of that well showed nitrites presence reflecting reducing conditions.
Key words: Mexico City, Chichinautzin ravine, hydrogeochemistry, nitrates, nitrites.
INTRODUCCION
Los nitratos se encuentran naturalmente en muchos ecosistemas acuáticos en moderada cantidad. En el agua subterránea pueden relacionarse con actividades volcánicas y procesos de consolidación de sedimentos (Strathouse et al. 1980). Sin embargo, determinadas actividades antrópicas, principalmente asociadas a la agricultura y excretas animales, contribuyen a que sus niveles se eleven considerablemente.
La concentración máxima permisible de N-NO3-en agua de consumo es de 10 mg/L (44.26 mg/L expresado como NO3-), de acuerdo con lo establecido por la norma mexicana, NOM-127-SSA1-1994 (SSA 2000). Se ha encontrado que concentraciones por arriba de esta norma originan metahemoglobinemia en infantes y otros problemas de salud en adultos debido a su transformación en nitritos por participación de bacterias existentes en el estómago y vejiga urinaria (Mirvish 1977, Bartsch y Montesano 1984, Crespi y Ramazzotti 1991, Tsezou et al. 1996). A su vez los nitritos se transforman en nitrosaminas que afectan al estómago e hígado, pudiendo originar cáncer (Mirvish 1991, Lee et al. 1992, Weyer 2001, Wolfey Patz 2002). En mujeres embarazadas, atraviesan la placenta y están asociados a defectos del nacimiento, como paladar hendido o defectos del tubo neural por lo que es importante tomar las medidas adecuadas a fin de controlar y posteriormente disminuir su concentración (Smolders et al. 2010).
La infiltración de nitratos al agua subterránea es un proceso complejo que depende de muchos factores (Almasri 2007) como el uso y características del suelo, carga de nitrógeno presente en el mismo, zonas de recarga de agua subterránea y la profundidad del nivel freático (Birkinshaw y Ewen 2000, Vinten y Dunn 2001, Bekesi y McConchie 2002).
La contaminación por nitratos en acuíferos ha sido ampliamente estudiada y analizada en el mundo (Styczen y Storm 1993, Hubbard y Sheridan 1994, Callesen et al. 1999, Nolan 2001, Rodvang y Simpinks 2001, Kunkel et al. 2004, Zotarelli et al. 2007). Debido a su gran movilidad en el agua estos iones se infiltran fácilmente hacia los acuíferos y por lo tanto constituyen el contaminante químico más encontrado en los cuerpos de agua (Spalding y Exner 1993).
Se han realizado diversos estudios relacionados con la presencia de nitratos en la Cuenca de México. Ryan (1989) identificó contaminación por nitratos en el sur de la Cuenca y determinó aportes por agua residual en áreas con gradientes hidráulicos descendentes o en áreas de recarga. Las mayores concentraciones de nitratos se detectaron en la periferia de la zona arcillosa. Lesser y asociados (1993) encontraron contenidos elevados de nitratos y color asociados a fosas sépticas en las áreas de Tlalpan, y en algunos pozos del ramal Tláhuac-Neza altos niveles de nitrógeno proteico y amoniacal, cuyas fuentes son la degradación de la materia orgánica de las arcillas lacustres y el aporte de agua proveniente de las arcillas.
En cuanto a las condiciones redox y de saturación prevalecientes, Ryan (1989) ratifica que, a medida que se produce el cambio de condiciones de acuífero libre a confinado, el potencial de óxido reducción disminuye notablemente. Edmunds et al. (2002) establecen la presencia de una barrera redox en la dirección del flujo subterráneo que, en el caso de nitratos, se relaciona con su disminución. Se ha reportado también que a medida que se produce el cambio de condiciones de acuífero libre a semiconfinado, el potencial de óxido reducción y las condiciones de saturación disminuyen notablemente y que las especies reducidas son más abundantes en la región semiconfinada (Cardona y Hernández 1995).
Armienta y Rodríguez (2011) determinaron presencia de nitratos en pozos de abastecimiento de agua potable en áreas dentro del suroeste del Distrito Federal y estribaciones de la Sierra Chichinautzin. En relación al límite máximo permisible para agua potable, las concentraciones de nitratos en la mayoría de los sitios se encontraron aún por debajo del mismo. El presente trabajo tiene como objetivo determinar la distribución espacial de los nitratos y su relación con la evolución hidrogeoquímica de los iones mayores y las condiciones hidrogeológicas de la zona de estudio.
ASPECTOS GENERALES DE LA ZONA DE ESTUDIO
La Ciudad de México se encuentra en parte de la superficie de la Cuenca de México, a una altitud promedio entre 2240 y 2390 msnm en lo que alguna vez fueron los lagos de Texcoco, Xochimilco y Chalco. Es una región geográfica con importantes implicaciones y cuyos acuíferos han sido intensamente estudiados (Vázquez-Sánchez y Jaimes-Palomera 1989, Birkle et al. 1995, Durazo 1996, Campos et al. 1997, González-Morán et al. 1999, Soto et al. 2000, Izazola 2001, Edmunds et al. 2002, Huizar et al. 2004, Carrera-Hernández y Gaskin 2007, 2008, Ramos-Leal et al. 2010) y explotados.
Debido a las severas alteraciones hidrológicas y ecológicas en la planicie de México, casi la totalidad de sus lagos se han desecado. Esta situación ha inducido cambios en las condiciones climáticas a niveles regional y microrregional (Jáuregui 2005).
La cuenca de México pertenece a las planicies escalonadas que forman parte del Arco Volcánico Trans-Americano (Damon et al. 1981). Es una extensa altiplanicie lacustre rodeada por sierras volcánicas y por abanicos y llanuras aluviales.
Existen formaciones geológicas originadas durante el Mioceno-Pleistoceno compuestas por andesitas, dacitas, riodacitas en las sierras de Las Cruces y Nevada y en el cerro Ajusco; del Plioceno-Pleistoceno hay basaltos y andesitas en el núcleo de la Sierra de Santa Catarina; del Cuaternario, también basaltos y andesitas, en la Sierra de Chichinautzin.
En el entorno de las sierras existen alternancias de derrames lávicos, piroclastos y cenizas (Rodríguez y Ochoa 1989) (Fig.1).
Desde el punto de vista hidrogeológico respecto a los pozos actualmente en explotación pueden señalarse dos estratos principales en la Cuenca. El acuitardo superior, formado principalmente por sedimentos lacustres fundamentalmente arcillosos, se extiende en toda la planicie lacustre hacia el centro de la planicie; y el acuífero superior, que es la principal unidad hidrogeológica en explotación, está constituido por materiales granulares y arcillosos y depósitos volcánicos de rocas basálticas y andesíticas fracturadas, con un espesor promedio de 400 m. Arcillas lacustres subyacen este acuífero (Mooser y Molina 1993, Ortega y Cherry 1993, Durazo 1996, Birkle et al. 1998, Huizar et al. 2004, Carrera-Hernández y Gaskin 2007).
Las zonas de recarga se encuentran en las áreas de las serranías meridionales. La mayor parte del flujo desde esta zona se desplaza en forma lateral descendente y hacia el sur de la Cuenca de México. Se ha determinado que la recarga en la Sierra de Chichinautzin es resultado de la presencia de fallas, mismas que evitan el drenaje natural fuera de la Cuenca hacia la parte norte del estado de Morelos (CAVM, DGCOH 1987, DGCOH 1993). Sin embargo, en la zona arcillosa el gradiente de flujo también puede ser inducido debido a bombeos intensos en el acuífero subyacente a la misma capa.
La zona del presente estudio se encuentra en la parte suroeste de la Cuenca de México, entre las coordenadas UTM 476758.51, 2126471.22 y 497500.85, 2135036.10, en parte de las delegaciones políticas Magdalena Contreras, Coyoacán, Tlalpan, Xochimilco y Tláhuac, cuya población aproximada es de 1 925 076 habitantes (INEGI 2010), con altitudes entre los 2237 y los 2432 msnm registradas en los pozos de muestreo (Fig. 2). Comprende aproximadamente 50 % de suelo urbano y 50 % de suelo de conservación, que se localiza en las últimas tres delegaciones mencionadas (Fig. 2) y abarca una superficie de 178 km2. Los límites de la zona son, al NW, la Avenida Periférico Sur en su cruce con Avenida Camino a Santa Teresa y al SE, la Carretera Tulyehualco-Tláhuac casi con Avenida Aquiles Serdán.
Esta región se encuentra inmersa en estructuras originadas durante el Cretácico, Terciario y Cuaternario, comprendiendo andesitas y basaltos pertenecientes a la formación Tarango y Chichinautzin y en la zona nororiental se presentan arcillas que pertenecen a los depósitos lacustres de la planicie.
MATERIALES Y MÉTODOS
Los datos utilizados para este trabajo provinieron de 42 pozos de agua potable pertenecientes al (SACM) Sistema de Aguas de la Ciudad de México (Fig. 3) cuyas muestras se recolectaron en abril del año 2011.
Los envases usados en el muestreo se lavaron varias veces con agua desionizada, enjuagándose con una solución de HCl al 10 %, y vueltos a enjuagar con agua desionizada. Los envases fueron de polietileno con tapa y contratapa de capacidades de 1 L y 500 mL.
Se realizaron colectas para la determinación de cloruros, sulfatos, alcalinidad, sodio, potasio, calcio, magnesio y nitratos. Las muestras destinadas al análisis de aniones (Cl-, CO32-, HCO3-, SO42-) se envasaron en frascos de polietileno de 1 L sin acidificar y de 500 mL para cationes (Na+, K+, Ca2+, Mg2+ ) en cada punto de muestreo. Las muestras que fueron analizadas por HPLC para la determinación de NO3- y NO2- se envasaron en frascos de polietileno de 500 mL sin añadir conservadores y se analizaron al siguiente día. Todas las muestras se almacenaron en hielo y se conservaron en refrigeración a menos de 4 °C de temperatura hasta su análisis en el laboratorio de Química Analítica del Instituto de Geofísica de la UNAM.
Determinaciones en campo
Las determinaciones de pH, conductividad eléctrica y temperatura se realizaron con una celda de flujo. Se utilizó un potenciómetro-conductímetro marca Conductronic modelo PC18 calibrándose con soluciones amortiguadoras de pH 7.01 y 4.01 para medición de pH y con solución de KCl de 1990 µS/cm para conductividad eléctrica.
Análisis químicos
Las concentraciones de iones mayores se determinaron siguiendo los procedimientos establecidos en APHA-AWWA-WPCF (2005). La alcalinidad se midió por volumetría mediante titulación con HCl. Los contenidos de cloruro se cuantificaron por potenciometría con electrodos selectivos, usando un equipo Thermo Orion 5-Stars y solución ajustadora de fuerza iónica. Los sulfatos se determinaron empleando el método turbidimétrico, para el cual se leyeron las absorbancias a 420 nm en un espectrofotómetro marca Hewlett Packard modelo 8452A. La cuantificación de sodio y potasio se realizó empleando emisión atómica con un espectrofotómetro de absorción atómica Perkin Elmer modelo AAnalyst100. Las concentraciones de Ca2+ y Mg2+ se determinaron mediante titulación con EDTA. Finalmente se calcularon los balances iónicos utilizando los equivalentes de cada especie con la siguiente fórmula:

La determinación de nitratos se realizó por HPLC con un equipo marca Waters con inyección manual y detector de conductividad Waters 432. Se utilizó una columna IC-Pak Anion HR de 4.6 x 75 mm filtrando las muestras al vacío con membranas de 0.45 µm. La fase móvil se preparó con un concentrado conteniendo hidróxido de litio, ácido bórico, ácido glucónico y glicerina. El concentrado se mezcló con acetonitrilo grado HPLC en una proporción de acetonitrilo correspondiente al 12 %. Se prepararon estándares para obtener una curva de calibración de cinco puntos. El límite de detección fue de 1 mg/L para NO3- y para NO2-.
Con objeto de visualizar fácilmente los pozos con distintas concentraciones de nitratos se establecieron siete rangos. Se eligió esta división ya que se trata de un submúltiplo entero del número de muestras (42) y permite identificar un conjunto de valores cercanos a la media. Se definieron los siguientes: Rango 1 (0-6.4 mg/L), Rango 2 (6.4-12.9 mg/L), Rango 3 (12.9-19.3 mg/L), Rango 4 (19.3-25.7 mg/L), Rango 5 (25.7-32.1 mg/L), Rango 6 (32.1-38.6 mg/L), Rango 7 (38.6-45 mg/L).
La representación gráfica de los resultados para establecer los tipos de agua predominantes se realizó por medio de la construcción de diagramas de Stiff y de Piper utilizados ampliamente en hidrogeoquímica (Piper 1944, Stiff1951, Custodio y Llamas 1976), que permiten identificar rápidamente la presencia y concentraciones de los iones Cl-, SO42-, HCO3-, CO32-, Na+, K+, Ca2+ y Mg2+ así como el posible origen del agua y su tiempo de permanencia en el acuífero.
Los diagramas de isoconcentraciones de cloruros y nitratos se realizaron con el programa Surfer versión 8.
Análisis multivariado
Con el fin de determinar las principales variables que explican los datos obtenidos, se realizó un análisis multivariado por medio del método de componentes principales, (Hotelling 1933). Los criterios en el manejo estadístico de los datos fueron los siguientes: se incluyeron las muestras de agua que tuvieron un balance iónico menor al 10 % y con varianza no nula (Cuadro I).

Se utilizó una rotación varimax y la determinación del número de componentes a utilizar se realizó por medio del criterio de Kaiser-Meyer-Olkin aplicando la prueba de esfericidad de Bartlett (Bartlett 1937).
Secciones geológicas. Se elaboraron dos perfiles geológicos con ayuda del programa AutoCad, considerando la información litológica proporcionada por el SACM y los planos constructivos de 30 pozos cercanos (a una distancia máxima de 100 m) a los ejes trazados. Estos ejes se definieron considerando posibles direcciones perpendiculares de flujo del agua subterránea (A-A" y B-B').
RESULTADOS Y DISCUSIÓN
Análisis de componentes principales
Los resultados de este análisis indican que existen dos componentes principales que explican el mayor porcentaje de la varianza. Estos son: el primero, la conductividad eléctrica con el 57.68 % y el segundo los iones nitrato y sulfato con 22.74 % (Cuadro II). A su vez, se establece que la conductividad eléctrica tiene una relación alta con los iones Mg2+, HCO3-, Na + y Ca2+ (Cuadro III).

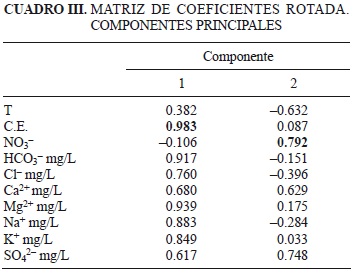
Esto es muy congruente debido a que la conductividad eléctrica depende de las concentraciones de iones disueltos en el agua. Por otra parte, la segunda componente, el ion NO3-, se encuentra relacionada con el ion SO42-; ambos iones pueden estar presentes en condiciones oxidantes y asociados a procesos biológicos. Sin embargo, los resultados estadísticos no brindan suficientes elementos para determinar los procesos que influyen en la presencia y distribución de los nitratos en el acuífero, por lo que se requiere interpretar las variaciones en las concentraciones de las especies químicas con un enfoque geoquímico en el contexto hidrogeológico.
Parámetros fisicoquímicos
En el cuadro IV se muestran los rangos de los análisis fisicoquímicos. Los valores de pH variaron de ligeramente ácidos a básicos dentro del rango establecido de 6.5 a 8.5 en la NOM-127-SSA1-1994 (SSA 2000). La conductividad eléctrica varió entre 161 y 743 µS/cm; la temperatura entre 13.2 y 24.3 °C.
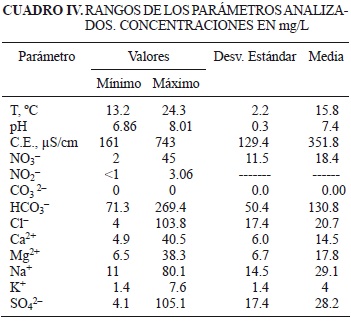
De entre los iones de mayor importancia en este artículo, los nitratos variaron entre 2 y 45 mg/L, los nitritos cuyos valores fueron desde menores al límite de detección hasta 3.06 mg/L, los HCO3- de 71.3 a 269.4 mg/L, los Cl- de 4 a 103.8 mg/L y los SO42- de 4.1 a 105.1 mg/L.
Análisis químicos
Todas las concentraciones de los iones principales fueron menores a los límites establecidos por la norma mencionada, ya que el Na+ fue menor a 80.1 mg/L, Ca2+ a 40.5 mg/L, Mg2+ a 38.3 mg/L, Cl- a 103.8 mg/L, y SO42- a 105.1 mg/L (datos en Cuadro IV). A partir de las concentraciones de estos iones y descartando los análisis de un pozo con balance iónico de 10.96 % se elaboró el diagrama de Piper (Fig. 4) en el cual se identifican aguas en su mayoría de tipo bicarbonatada mixta, y algunas que corresponden a bicarbonatada sódica, mixta-sódica y mixta-mixta ubicadas principalmente al noroeste de la zona de estudio en las inmediaciones de la zona de recarga. Esto indica trayectorias de flujo con tiempos de residencia recientes a intermedios, principalmente a través de las rocas volcánicas de la zona. Estos resultados concuerdan con los reportados por otros autores que han realizado estudios de composición del agua que abarcan esta zona (Cardona y Hernández 1995, Edmunds et al. 2002, Huizar et al. 2004).

En el cuadro V se observa que las concentraciones de N-NO3- son inferiores al límite establecido de 10 mg/L (44.26 mg/L expresado como NO3-) para casi todas las muestras; únicamente en una de ellas (S-10) se llega a dicho valor. Sin embargo, en cuatro sitios los valores (entre 30 y 45 mg/L de NO3-) se encuentran cercanos al límite permisible establecido en la norma oficial mencionada. Solamente se detectó la presencia de nitritos en un pozo (PS-1 con 3 mg/L de NO2-) y éste fue muy cercano al estándar para agua potable de 1 mg/L de N-NO2- (equivalente a 3.28 mg/L expresado como NO2-). La distribución espacial de las concentraciones de nitratos por rangos asignados, se muestra en la figura 5 y las tendencias espaciales de isoconcentraciones se muestran en la figura 6. En estas figuras se observa que la zona con menores concentraciones de nitratos está ubicada en el extremo noreste (NE) del eje B-B'. Asimismo, los mayores niveles se presentan en dos zonas que, aunque se encuentran en superficie urbana, están próximas a lugares que pudieran ser fuentes de agua contaminada hacia el acuífero, ya sea por fugas en el drenaje (Armienta y Rodríguez 2011), o bien debido a la presencia de ósfera, ya que estos compuestos nitrogenados han sido reportados en el análisis de partículas suspendidas menores a 10 mm por varios autores (Gutiérrez-Castillo et al. 2005, Volkamer et al. 2010) y pueden ser infiltrados en zonas con cubierta vegetal como parques y jardines debido a la lluvia o al riego.


Los pozos con presencia de compuestos nitrogenados se encuentran cercanos al eje A-A". El único pozo que rebasó la norma para consumo humano de 10 mg/L como N-NO3- (44.3 mg/L NO3-) fue el S-10, ubicado cerca del extremo suroeste (SO) del eje B-B'.
Internacionalmente se ha identificado que las fuentes de aporte de nitratos al agua subterránea son los fertilizantes utilizados en la agricultura, sobre todo en suelos arenosos (Postma et al. 1991, Pang y Letey 2000, Rodvang y Simpkins 2001, Babiker et al. 2004, Dunn et al. 2004, Jiao et al. 2004, Ju et al. 2006), las actividades ganaderas (Steele y McCalister 1991, Sloan et al. 1999, van Es et al. 2006, Singleton et al. 2007) y los asentamientos humanos, siendo estos últimos la fuente principal de aporte de nitratos al agua subterránea (Arnade 1999, MacQuarrie et al. 2001, Gardner y Vogel 2005), esto en parte causado por las fugas en los sistemas de drenaje (Robertson et al. 1991, Wilhelm et al. 1994, MacQuarrie et al. 2001, Wakida y Lerner 2005). Por otra parte se ha encontrado que la cantidad de nitrógeno total, presente en un agua residual doméstica promedio, es de 40 mg/L (Metcalf y Eddy 1991).
La existencia de asentamientos que carecen de drenaje en las faldas de la Sierra Chichinautzin (Aguilar y Santos 2011) podría indicar que la fuente de nitratos más probable es la infiltración de aguas residuales provenientes de los mismos.
La distribución observada en la figura 5 y la figura 6 podría entonces atribuirse a infiltraciones de aguas residuales procedentes de esta zona que corresponde al área de recarga. Cabe señalar que parte de esta área incluye al pie de monte que ha sido considerada de alta vulnerabilidad dentro de la Cuenca de México (Ramos-Leal et al. 2010), donde además, estudios previos (Mazari-Hiriart et al. 1999) identificaron contaminación por microorganismos patógenos en muestras de agua de pozos colectadas antes de la cloración.
Las tendencias de concentración de cloruros pueden utilizarse como indicadores de direcciones de flujo donde no existan fuentes adicionales de este ion (p. ej. intrusión salina, lixiviados de basureros, aguas geotérmicas); dado que el ión cloruro es uno de los mejores indicadores de la evolución química del agua subterránea en la Cuenca de México (Cardona y Hernández 1995) por ser el menos afectado por procesos de precipitación, adsorción o de óxido reducción y por viajar en el agua a la misma velocidad que ésta, al igual que los nitratos (no conservativos), se utiliza como trazador. Por otro lado, a pesar de que los nitratos son un contaminante muy móvil, principalmente en presencia de condiciones oxidantes en el agua, no pueden considerarse conservativos debido a que su concentración puede ser afectada por reacciones de nitrificación y desnitrificación en los acuíferos (Freeze y Cherry 1979).
Por lo anteriormente expuesto, se determinó el comportamiento del ion cloruro (Fig. 7) y se observa un incremento hacia el noreste y la presencia de un máximo en el área cercana a las avenidas Insurgentes y Periférico. Las concentraciones máximas de cloruros se registran en los pozos DF1135, DF1110, DF1134, DF1138 y DF1123 y los mínimos en DF1101, DF1112, DF1111 y DF1108 en la zona de San Lucas Xochimanca, delegación Xochimilco. La tendencia general es a incrementarse en dirección radial hacia la planicie, lo que refleja la dirección del flujo del agua subterránea a partir de la Sierra Chichinautzin hacia el centro del valle.

Secciones geológicas
Las profundidades de los pozos seleccionados para elaborar las secciones geológicas (Fig. 8 y Fig. 9) varían de 31 a 330 m y sus elevaciones oscilan entre los 2237 y los 2431 msnm. El nivel dinámico de los pozos analizados atraviesa por basaltos, cenizas volcánicas, gravas y arenas pertenecientes a la formación Tarango, así como arcillas lacustres (Cuadro VI).

En la sección A-A' se observa la presencia de rocas volcánicas en la zona montañosa (identificados en la mayoría de los pozos) que se han reportado como fracturados (Carrera-Hernández y Gaskin 2007) y que facilitan la infiltración del agua hacia el acuífero. Por otro lado, se observan zonas de arcilla solamente en los pozos ubicados en el área de Xochimilco más alejadas de la zona montañosa.
Debido a que el eje B-B' parte de la zona cercana a la estribaciones de la Sierra Chichinahutzin, hacia el centro de la planicie, se consideró para determinar las variaciones en las concentraciones de los iones a lo largo del flujo. Se seleccionaron los pozos sobre los cuales se estima que el agua subterránea transita paralelamente al eje B-B' cercanos al mismo (pozos DF1129, DF1128, DF1127, DF1126, DF1125, DF1124 y DF1122).
El perfil muestra un incremento en la conductividad eléctrica a lo largo del eje B-B' (Fig. 9). La misma tendencia (aumento hacia el noreste) se observa para las concentraciones de los iones sodio, cloruro y bicarbonatos que se refleja en los diagramas de Stiff mostrados en esta figura. Por otro lado, tanto los nitratos como los sulfatos muestran una tendencia similar con concentraciones menores en la zona noreste.
De acuerdo con la fitología del acuífero (Cuadro VI), con la familia de agua prevaleciente, también conocida como facie hidrogeoquímica reflejada en el diagrama de Piper (Fig. 4), y con los bajos valores de los parámetros físico-químicos temperatura, conductividad eléctrica y iones disueltos ( Cuadro IV), así como a su variación, se determina que estas aguas no tienen tiempos de residencia largos en el acuífero, principalmente en la Sierra Chichinautzin.
La persistencia de concentraciones bajas de iones mayores y el predominio de bicarbonatos refleja poco tiempo de interacción agua-roca e indica una alta permeabilidad por fisuración sobre todo de las rocas volcánicas del área.
Conforme va disminuyendo el potencial de óxido reducción en la dirección del flujo, puede efectuarse la reducción de especies nitrogenadas (desnitrificación), ya que la acción de las bacterias desnitrificantes depende de factores como la disponibilidad de oxígeno y la concentración de donadores de electrones (Rivett et al. 2008). En la figura 9 se observa que la relación NO3-:Cl- (en meq/L) presenta una tendencia decreciente hacia el noreste, lo que sugiere que a lo largo del flujo (en la sección B-B') disminuyen los contenidos de NO3- debido a condiciones menos oxidantes.
Cardona y Hernández (1995) mencionan que la disminución del nitrógeno como nitrato en la zona reductora del acuífero de la Cuenca de México parece estar relacionada con el desarrollo de reacciones de desnitrificación particularmente en la región donde el acuífero cambia de libre a semiconfinado. La presencia de nitritos determinada únicamente en el pozo más alejado de la zona de recarga muestreada en este trabajo, probablemente ubicado en las inmediaciones o dentro de la zona confinada, confirma las observaciones señaladas por dichos autores. Por otro lado, Sparks (1987), a partir del estudio de nueve tipos de suelos observó un incremento en la capacidad de intercambio aniónico con la profundidad al aumentar el contenido de arcillas y óxidos. La retención de nitratos mostró correlaciones muy fuertes con dichos contenidos. Este proceso podría también ocurrir en la zona noreste de la sección B-B' con presencia de arcillas lacustres.
CONCLUSIONES
En la zona de estudio se detectó presencia de nitratos que indican procesos de contaminación, aunque solamente en un pozo se rebasó la norma de calidad para agua potable de 10 mg/L de N-NO3- con un valor de 10.16 mg/L (SSA 2000). En cuanto a la presencia de nitritos, éstos sólo se encontraron en la zona más lejana de infiltración del agua al medio (pozo PS-1 con un valor de 3 mg/L de NO2-), zona en la que se encuentra ya una cantidad importante de arcillas lacustres y que, debido al comportamiento de los sulfatos, bicarbonatos y nitratos sugiere condiciones reductoras en el medio. Se encontraron dos zonas con las mayores concentraciones de nitratos y cloruros, localizada la primera muy cerca de la Avenida Periférico en Tepepan, Xochimilco, al sureste del eje B-B' y la otra cercana al cruce de las avenidas Periférico e Insurgentes, respectivamente.
Se observó una distribución de nitratos que tiende a decrecer conforme el flujo de agua avanza en la planicie hacia la zona lacustre, proviniendo de la zona de recarga en el acuífero fracturado. Esta disminución sugiere el cambio de condiciones oxidantes a reductoras con la presencia de arcillas lacustres en el pozo DF 1122 localizado en la parte más nororiental del eje longitudinal al flujo (B-B').
La tendencia creciente de las concentraciones de los iones de Na+ y Cl- y de la conductividad eléctrica del agua graficados sobre el eje a lo largo de la dirección del flujo indica que el agua subterránea en las faldas de Chichinautzin se mueve en sentido radial hacia la planicie.
El decremento observado de los nitratos, la presencia de nitritos en uno de los pozos más alejados de la zona de recarga, y su relación con la geología indican que se podrían estar efectuando procesos de reducción y/o adsorción. Esta hipótesis y la concerniente al desarrollo de reacciones de desnitrificación deberán demostrarse con estudios más detallados que incluyan determinaciones isotópicas y modelaciones hidrogeoquímicas.
AGRADECIMIENTOS
Al Instituto de Ciencia y Tecnología del D.F. por el financiamiento del proyecto "Monitoreo específico de agua subterránea en el Sur-Oeste de la zona metropolitana de la cuenca de México". A Alejandro Escobedo Ramírez del SACM por la información facilitada, a Alejandra Aguayo, Nora Ceniceros, Olivia Cruz R. y Omar Neri del Laboratorio de Química Analítica del IGF por su importante participación en el análisis de muestras, al Consejo Nacional de Ciencia y Tecnología por la beca otorgada a la primera autora para realizar el posgrado, y al Sistema de Aguas de la Ciudad de México por facilitar el acceso a los pozos para realizar el muestreo.
REFERENCIAS
Aguilar A.G. y Santos C. (2011). Informal settlements' needs and environmental conservation in Mexico City: An unsolved challenge for land-use policy. Land Use Policy 28, 649-662. [ Links ]
Almasri M.N. (2007). Nitrate contamination of groundwater: A conceptual management framework. Environ. Impact Asses. 27, 220-242. [ Links ]
APHA-AWWA-WPCF (2005). Standard Methods for the Examination of Water and Wastewater. 2 ed., Washington, EUA, 1320 pp. [ Links ]
Armienta M.A. y Rodríguez C.R. (2011). Monitoreo específico de agua subterránea en el sur-oeste de la Zona Metropolitana de la Cuenca de México. Instituto de Ciencia y Tecnología del Distrito Federal, Instituto de Geofísica, UNAM, Reporte, México, D.F. 84 pp. [ Links ]
Arnade L.J. (1999). Seasonal correlation of well contamination and septic tank distance. Ground Water 37, 920-923. [ Links ]
Babiker I.S., Mohamed M.A.A., Terao H., Kato K. y Ohta K. (2004). Assessment of groundwater contamination by nitrate leaching from intensive vegetable cultivation using geographical information system. Environ. Int. 29, 1009-1017. [ Links ]
Bartlett M.S. (1937). Properties of sufficiency and statistical tests. Proc. R. Soc. Lond. A. 160, 268-282. [ Links ]
Bartsch H. y Montesano R. (1984). Relevance of nitrosamines to human cancer. Carcinogenesis 5, 1381-1393. [ Links ]
Bekesi G. y McConchie J. (2002). The use of aquifer-media characteristics to model vulnerability to contamination, Manawatu region, New Zealand. Hydrogeol. J. 10, 322-331. [ Links ]
Birkinshaw S.J. y Ewen J. (2000). Nitrogen transformation component for SHETRAN catchment nitrate transport modelling. J. Hydrol. 230, 1-17. [ Links ]
Birkle P., Torres R. V. y González-Partida E. (1995). Evaluación preliminar del potencial de acuíferos profundos en la Cuenca del Valle de México. Ing. Hidraul. Mex. 10, 47-53. [ Links ]
Birkle P., Torres-Rodríguez V. y González Partida E. (1998). The water balance for the Basin of the Valley of Mexico and implications for future water consumption. Hydrogeol. J. 6, 500-517. [ Links ]
Callesen I., Rauland-Rasmussen K., Gundersen P. y Stryhn H. (1999). Nitrate concentrations in soil solutions below Danish forests. Forest Ecol. Manag. 114, 71-82. [ Links ]
Campos J.O., Delgado-Rodríguez O., Chávez R., Gómez P., Flores E.L. y Birch F.S. (1997). The subsurface structure of the Chalco sub-basin (Mexico City) inferred from geophysical data. Geophysics 62, 23-35. [ Links ]
Cardona A. y Hernández N. (1995). Modelo geoquímico conceptual de la evolución del agua subterránea en al Valle de México. Ing. Hidraul. Mex. 10, 71-90. [ Links ]
Carrera-Hernández J. J. y Gaskin S. J. (2007). The basin of Mexico aquifer system: regional groundwater level dynamics and database development. Hydrogeol. J. 15, 1577-1590. [ Links ]
Carrera-Hernández J.J. y Gaskin S.J. (2008). Spatio-temporal analysis of potential aquifer recharge: Application to the Basin of Mexico. J. Hydrol. 353, 228-246. [ Links ]
CAVM, DGCOH (1987). Análisis de flujo de aguas subterráneas del Valle de México mediante trazadores isotópicos. Sistema de Aguas de la Ciudad de México. Informe del IGF a la SARH, CAVM, mayo 1987. México, D.F. 64 pp. [ Links ]
Crespi M. y Ramazzotti V. (1991). Evidence that N-nitroso compounds contribute to the causation of certain human cancers. En: Nitrate contamination: Exposure, consequence, and control (I. Bogardi, R.D. Kuzelka, W.G. Ennenga, Eds.). NATO ASI S. G: Ecological Sciences 30; Springer-Verlag, Berlin, Alemania, pp. 233-252. [ Links ]
Custodio G.E. y Llamas M.R. (1976). Hidrología subterránea. Omega, Barcelona, España, 1194 pp. [ Links ]
Damon P.E., Shafiqullah M. y Clark K.F. (1981). Evolución de los arcos magmáticos en México y su relación con la metalogénesis. Rev. Mex. Cienc. Geol. 5, 223-238. [ Links ]
DGCOH (1993). Suministro de agua potable en la ciudad de México. Memorias del IX Congreso Nacional de Ingeniería Sanitaria y Ambiental y I Congreso Internacional AIDIS de Norteamérica y del Caribe. Sistema de Aguas de la Ciudad de México, Dirección General de Construcción y Operación Hidráulica, México, D.F., 11 al 16 de octubre, 1993. pp 7-9. [ Links ]
Dunn S.M., Lilly A., DeGroote J. y Vinten A.A. (2004). Nitrogen risk assessment model for Scotland: II. Hydrological transport and model testing. Hydrol. Earth Syst. Sc. 8, 205-219. [ Links ]
Durazo J. (1996). Ciudad de México, acuitardo superficial y contaminación acuífera. Ing. Hidraul. Mex. 11, 5-14. [ Links ]
Edmunds W.M., Carrillo-Rivera J.J. y Cardona A. (2002). Geochemical evolution of groundwater beneath Mexico City. J. Hydrol. 258, 1-24. [ Links ]
Freeze R.A. y Cherry J.A. (1979). Groundwater. Prentice-Hall, Englewood Cliffs N. J., EUA, 604 pp. [ Links ]
Gardner K.K. y Vogel R.M. (2005). Predicting ground water nitrate concentrations from land use. Ground Water 43, 343-352. [ Links ]
González-Morán T., Rodríguez R. y Cortés S.A. (1999). The basin of Mexico and its metropolitan area: water abstraction and related environmental problems. J. S. Am. Earth Sci. 12, 607-613. [ Links ]
Gutiérrez-Castillo M.E., Olivos-Ortiz M., De Vizcaya-Ruiz, A. y Cebrian M.E. (2005). Chemical characterization of extractable water soluble matter associated with PM10 from Mexico City during 2000. Chemosphere 61, 701-710. [ Links ]
Hotelling H. (1933). Analysis of a complex of statistical variables with principal componentes. J. Educ. Psychol. 24, 417-441. [ Links ]
Hubbard R.K. y Sheridan J.M. (1994). Nitrates in ground-water in the Southeastern USA. En: Contamination of groundwaters, Science Reviews (D.C. Adriano, A. K. Iskandar e I. P. Murarka, Eds.). Northwood, Inglaterra, pp. 303-345. [ Links ]
Huizar A.R., Carrillo-Rivera J.J., Angeles-Serrano G., Hergt T. y Cardona A. (2004). Chemical response to groundwater extraction southeast of Mexico City. Hydrogeol. J. 12, 436-450. [ Links ]
INEGI (2010). Censo de Población y Vivienda. Instituto Nacional de Estadística y Geografía, México. [ Links ]
Izazola H. (2001). Agua y sustentabilidad en la Ciudad de México. Estudios Demográficos y Urbanos 47, 285-320. [ Links ]
Jáuregui O.E. (2005). Possible impact of urbanization on the thermal climate of some large cities in Mexico. Atmósfera 18, 249-252. [ Links ]
Jiao Y., Hendershot W.H. y Whalen J.K. (2004). Agricultural practices influence dissolved nutrients leaching through intact soil cores. Soil Sci. Soc. Am. J., 68, 2058-2068. [ Links ]
Ju X.T., Kou C.L., Zhang F.S. y Christie P. (2006). Nitrogen balance and groundwater nitrate contamination. Comparison among three intensive cropping systems on the North China Plain. Environ. Pollut. 143, 117-125. [ Links ]
Kunkel R., Bach M., Behrendt H. y Wendland F. (2004). Groundwater-borne nitrate intakes into surface waters in Germany. Water Sci. Technol. 49, 11-19. [ Links ]
Lee Y.W., Dahab M.F. y Bogardi I. (1992). Nirate risk management under uncertainty. Plann. Manage 118, 151-165. [ Links ]
Lesser y Asociados (1993). Fuentes de contaminación al agua subterránea y alternativas de saneamiento. Departamento del Distrito Federal, Dirección General de Construcción y Operación Hidráulica, Reporte, México, D.F., 110 pp. [ Links ]
MacQuarrie K.T.B., Sudicky E. y Robertson W.D. (2001). Numerical simulation of a fine-grained denitrification layer for removing septic system nitrate from shallow groundwater. J. Hydrol. 52, 29-55. [ Links ]
Mazari-Hiriart M., Torres-Beristain B., Velázquez E., Calva J.J. y Pillai S.D. (1999). Bacterial and viral indicators of fecal pollution in Mexico City's southern aquifer. J. Env. Sci. Heal. A 34, 1715-1735. [ Links ]
Metcalf y Eddy (1991). Wastewater engineering. Treatment, disposal and reuse. 3a. ed. Mc Graw Hill, Nueva York, EUA, 1820 pp. [ Links ]
Mirvish S.S. (1977). N-nitroso compounds: their chemical and in vivo formation and possible importante as environmental carcinogens. J. Toxicol. Env. Health 2, 1267-1277. [ Links ]
Mirvish S.S. (1991). The significance for human health of nitrate, nitrite and N-nitroso compounds. En: Nitrate contamination: Exposure, consequence, and control. (I. Bogardi, R.D. Kuzelka y W.G. Ennenga, Eds.). NATO ASI S. G: Ecological Sciences 30; Springer-Verlag, Berlín, Alemania, pp. 253-266. [ Links ]
Mooser F. y Molina C. (1993). Nuevo modelo hidrogeológico para la Cuenca de México. Boletín del Centro de Investigación Sísmica de la Fundación Javier Barros Sierra. México, D.F. 3, 68-84. [ Links ]
Nolan T.B. (2001). Relating nitrogen sources and aquifer susceptibility to nitrate in shallow ground waters of de United States. Ground Water 39, 290-299. [ Links ]
Ortega G.A., Cherry J. y Rudolph D. (1993). Large scale aquitard consolidation near Mexico City. Ground Water 31, 708-718. [ Links ]
Pang X.P. y Letey J. (2000). Organic farming: Challenge of timing nitrogen availability to crop nitrogen requirements. Soil Sci. Soc. Am. J. 64, 247-253. [ Links ]
Piper A.M. (1944). A graphic procedure in the geochemical interpretation of water analyses. Trans. Amer. Geophys. Union 25, 914-923. [ Links ]
Postma D., Boesen C., Kristiansen H. y Larsen F. (1991). Nitrate reduction in an unconfined sandy aquifer: water chemistry, reduction processes, and geochemical modeling. Water Resour. Res. 27, 2027-2045. [ Links ]
Ramos-Leal J.A., Noyola-Medrano C. y Tapia-Silva F.O. (2010). Aquifer vulnerability and groundwater quality in mega cities: case of the Mexico Basin. Environ. Earth Sci. 61, 1309-1320. [ Links ]
Rivett M.O., Buss S.R., Morgan P., Smith J.W.N. y Bemment C.D. (2008). Nitrate attenuation in groundwater: a review of biogeochemical controlling processes. Water Res. 42, 4215-4232. [ Links ]
Robertson W.D., Cherry J.A. y Sudicky E.A. (1991). Ground-water contamination from two small septic systems on sand aquifers. Ground Water 29, 82-92. [ Links ]
Rodríguez C.R. y Ochoa A.C. (1989). Estudio geoeléctrico del sistema acuífero de la Cuenca de México. Geofis. Int. 28, 191-205. [ Links ]
Rodvang S. y Simpkins W. (2001). Agricultural contaminants in Quaternary aquitards: A review of occurrence and fate in North America. Hydrogeol. J. 9, 44-59. [ Links ]
Ryan M.C. (1989). An investigation of inorganic nitrogen compounds in the groundwater in the Valley of Mexico. Geofís. Int. 28, 417-433. [ Links ]
SGM (2002). Carta geológico-minera. Ciudad de México E14-2. Edo. de Méx., Tlax., D.F., Pue., Hgo. y Mor. Escala 1:250, 000: Pachuca, Hidalgo. México. Servicio Geológico Mexicano, 1 mapa. [ Links ]
Singleton M.J., Esser B.K., Moran J.E., Hudson G.B., McNab W.W. y Harter T. (2007). Saturated zone denitrification: Potential for natural attenuation of nitrate contamination in shallow groundwater under dairy operations. Environ. Sci. Technol. 41, 759-765. [ Links ]
Sloan A.J., Gilliam J.W., Parsons J.E., Mikkelson R.L. y Riley R.C. (1999). Ground water nitrate depletion in a swine-lagoon-effluent-irrigated pasture and adjacent riparian area. J. Soil Water Conserv. 54, 651-656. [ Links ]
Smolders A.J.P., Lucassen E.C.H.E.T., Bobbink R., Roelofs J.G.M. y Lamers L.P.M. (2010). How nitrate leaching from agricultural lands provokes phosphate eutrophication in groundwater fed wetlands: the sulphur bridge. Biogeochemistry 98, 1-7. [ Links ]
Soto G.E., Mazari H. y Bojórquez T.L.A. (2000). Entidades de la Zona Metropolitana de la Ciudad de México propensas a la contaminación de agua subterránea. Boletín IGg, 43, 60-75. [ Links ]
Spalding R.F. y Exner M.E. (1993). Occurrence of nitrate in ground water - a review. J. Environ. Qual. 22, 392-402. [ Links ]
Sparks D.L. (1987). Nitrate retention as it affects groundwater pollution in Mid-Atlantic soils. USGS, Reston, EUA, 46 pp. [ Links ]
SSA (2000). Modificación a la Norma Oficial Mexicana NOM-127-SSA1-1994. Salud ambiental. Agua para uso y consumo humano. Límites permisibles de calidad y tratamientos a que debe someterse el agua para su potabilización. Secretaría de Salubridad. Diario Oficial de la Federación, 22 de noviembre de 2000. [ Links ]
Steele K.F. y McCalister W.K. (1991). Potential nitrate pollution of ground water in limestone terrain by poultry litter, Ozark region, USA. En: Nitrate contamination: Exposure, consequence, and control. (I. Bogardi, R.D. Kuzelka y W.G. Ennenga, Eds.). NATO ASI S. G: Ecological Sciences 30; Springer-Verlag, Berlin, Alemania, pp. 209-218. [ Links ]
Starthouse M.S., Sposito G., Sullivan P.J. y Lund L.J. (1980). Geologic nitrogen: a potential geochemical hazard in the San Joaquin Valley, California. J. Environ. Qual. 9, 54-60. [ Links ]
Stiff H.A. Jr. (1951). The interpretation of chemical water analysis by means of patterns. J. Petrol. Technol. 3, 15-17. [ Links ]
Styczen M. y Storm B. (1993). Modelling of N-movements on catchment scale-a tool for analysis and decision making:1. Model description. Fert. Res. 36, 1-6. [ Links ]
Tsezou A., Kitsiou-Tzeli S., Galla A., Gourgiotis D., Papageorgiou J., Mitrou S., Molybdas P.A. y Sinaniotis C. (1996). High nitrate content in drinking water: cytogenetic effects in exposed children. Arch. Environ. Helath 51, 458-461. [ Links ]
van Es H.M, Sogbedji J.M. y Schindelbeck R.R. (2006). Effect of manure application timing, crop, and soil type on nitrate leaching. J. Environ. Qual. 35, 670-679. [ Links ]
Vázquez-Sánchez E. y Jaimes-Palomera R. (1989). Geología de la Cuenca de México. Geofís. Int. 28, 133-189. [ Links ]
Vinten A.J.A. y Dunn S.M. (2001). Assessing the effects of land use on temporal change in well water quality in a designated nitrate vulnerable zone. Sci. Total Environ. 265, 253-268. [ Links ]
Volkamer R., Sheehy P., Molina L.T. y Molina M.J. Oxidative capacity of the Mexico City atmosphere - Part 1: A radical source perspective 2010. Atmos. Chem. Phys. 10, 6969-6991. [ Links ]
Wakida F.T. y Lerner D.N. (2005). Non-agricultural sources of groundwater nitrate: a review and case study. Water Res. 39, 3-16. [ Links ]
Weyer P. (2001). Municipal drinking water nitrate level and cancer risk in older women: the Iowa women's health study. Epidemiology 12, 327-338. [ Links ]
Wilhelm S.R., Schiff S.L. y Robertson W.D. (1994). Chemical fate and transport in a domestic septic system: unsaturated and saturated zone geochemistry. Environ. Toxicol. Chem. 13, 193-203. [ Links ]
Wolfe A.H. y Patz J.A. (2002). Reactive nitrogen and human health: acute and longterm implications. AMBIO 31, 120-125. [ Links ]
Zotarelli L., Scholberg J.M., Dukes M.D. y Muñoz-Carpena R. (2007). Monitoring of nitrate leaching in sandy soils: Comparison of three methods. J. Environ. Qual. 36, 953-962. [ Links ]














