Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Acta pediátrica de México
versión On-line ISSN 2395-8235versión impresa ISSN 0186-2391
Acta pediatr. Méx vol.35 no.1 México ene./feb. 2014
Artículo original
Conexión anómala total de venas pulmonares a la vena porta. Valor de la angiotomografía multicorte. Informe de tres casos
Total anomalous pulmonary veins to the portal vein. Value of multislice CT angiography. Report of three cases
Sara Alejandra Solórzano-Morales,1 Francisco Javier López-Elías,1 Javier Horacio López-Terrazas,2 Max Alberto Bernal-Moreno,1 Alexis Javier Palacios-Macedo-Quenot,2 Alfredo Bobadilla-Aguirre3
1 Servicio de Radiología.
2 Cirugía Cardiovascular.
3 Servicio de Cardiología. Instituto Nacional de Pediatría, México DF.
Correspondencia
Dra. Sara Alejandra Solórzano Morales
Av. Insurgentes Sur 3700-C
04530 México DF
dras.solorzano@yahoo.com.mx
Recibido: septiembre, 2013
Aceptado: noviembre, 2013
RESUMEN
Objetivo: exponer los datos tomográficos de las pacientes con hincapié en las características estructurales.
Material y método: estudios retrospectivo de tres pacientes en quienes las cuatro venas pulmonares conectaban con la vena porta. Esta malformación es una de las variedades de conexión anómala total de las venas pulmonares. En cualquiera de ellas, las venas pulmonares no conectan con la aurícula izquierda y la sangre proveniente del pulmón llega a la aurícula derecha de manera directa o a través de sus sistemas tributarios. En estos casos, la sangre pulmonar arterializada y la sangre venosa sistémica se mezclan en el sitio de la conexión anómala y se establece un cortocircuito de la aurícula derecha a la aurícula izquierda a través de una comunicación interauricular, lo que permite que los pacientes sobrevivan.
La conexión anómala total de las venas pulmonares constituye entre 0.4 y 2.0% de las cardiopatías congénitas: ocurre en 6.8 de cada 100,000 individuos. Se diagnostica en 68% de los pacientes en etapa neonatal, lo que refleja la gravedad de esta cardiopatía. La variedad de conexión anómala total de las venas pulmonares infracardiaca representa entre 15 y 26% de todas sus variedades.
La angiotomografía multicorte permite visualizar los vasos y órganos vecinos en estudio y obtener información anatómica de alta definición. En las pacientes de este estudio la conexión anómala total de las venas pulmonares a la vena porta se visualizó con reconstrucciones tridimensionales volumétricas tomográficas y su correlación con estudios ultrasonográficos.
Palabras clave: conexión anómala total de venas pulmonares, cardiopatía congénita, angiotomografía, ultrasonografía.
ABSTRACT
We present three female patients with infracardiac total anomalous pulmonary venous connection (TAPVC) with the portal vein.
Angio CT scan reconstructions and a correlation between tomographic and echocardiographic findings were conducted.
Multi-slice angio CT scan has been a valuable tool for the study of vessels in children with congenital heart disease. It is performed rapidly and it obtains high quality images, showing the vessels and the adjacent organs, which supply excellent information.
The term TAPVC includes a group of malformations in which the four pulmonary veins connect in such a way that the arterialized blood in the lungs drains into the right atrium, either directly or by way of tributary veins. Thus, systemic and pulmonary blood mix in the right atrium; and atrial septal defect must exist in order for patients to survive.
These malformations represent 0.4 to 2.0 % of all congenital heart diseases, with an incidence of 6.8 patients in every 100,000 births. Sixty eight percent of the cases are diagnosed in newborns, which indicates that most patients are symptomatic early in life. The infracardiac TAPVC represent 15 to 25% of all TAPVC.
Key words: Total anomalous pulmonary venous connection; congenital heart disease; multi-slice CT scan; ultrasonography.
La primera descripción de un caso de conexión anómala total de las venas pulmonares la hizo Wilson en 1798. Las primeras sistematizaciones basadas en la embriología las realizaron Nelly, Edwards y Helmoltz en 1956, Darling en 1957 y Van Praag en 1969.1 Darling las dividió en supracardiacas, cardiacas, infracardiacas y mixtas. (Cuadro 1)
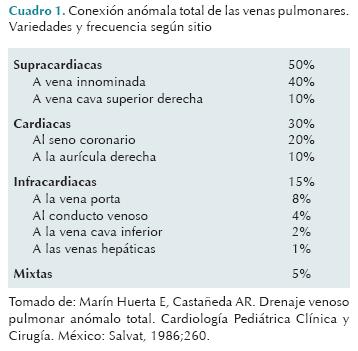
Las infracardiacas suelen ser las más graves. Todas requieren tratamiento quirúrgico temprano. El diagnóstico clínico es difícil; para establecerlo se requieren estudios altamente especializados que proporcionen datos precisos, como se hizo en nuestras pacientes: angiotomografía multicorte y ultrasonido Doppler color.
La gravedad de la malformación en nuestras pacientes no permitió recurrir al tratamiento quirúrgico; las tres fallecieron a pesar del tratamiento médico.
El objetivo de esta comunicación es exponer los datos tomográficos de las pacientes con hincapié en las características estructurales.
PACIENTES Y MÉTODO
Estudio retrospectivo de pacientes atendidas en el servicio de Cardiología del Instituto Nacional de Pediatría entre los años 2003 y 2011. Se encontraron tres casos de niñas con conexión anómala total de las venas pulmonares infracardiacas, con drenaje a la vena porta, estudiadas con angiotomografía y ultrasonido.
Los estudios tomográficos se hicieron en equipos de tomografía multicorte Siemens Sensetion de 4 y 64 filas de detectores. Se administró material de contraste hidrosoluble no iónico a dosis de 2 mL/kg a través de una vena periférica de un miembro inferior, con técnica de bolus-tracking en dirección craneocaudal (fase arterial) y caudo-craneal (venosa); grosor de corte 1-1.25 mm, PICH 1.0, MSA: 120, KVP: 80. Estos parámetros variaron en relación con la edad y peso de las pacientes. Las imágenes se evaluaron con reconstrucciones de máxima intensidad de proyección y tridimensionales volumétricas. Los estudios de ultrasonido se efectuaron con equipo General Electric LOGIQ P9 y HDL 5000.
CASOS CLÍNICOS
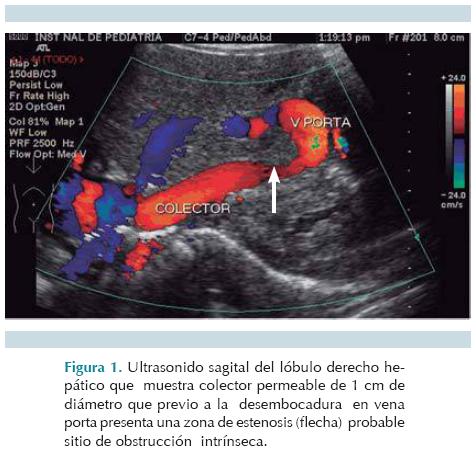
Caso 1. Niña de 2 meses de edad, sin antecedentes perinatales de interés. Cinco días antes tuvo disnea y cianosis. Se le había tratado inicialmente en otro centro hospitalario como neumonía. El ecocardiograma mostró dextroisomerismo, yuxtaposición aorto-cava, dos comunicaciones interauriculares, una tipo ostium primiun de 6 mm y otra tipo ostium secundum de 7 mm. Había un colector venoso con drenaje infradiafragmático; no se especificó el sitio de drenaje. El cateterismo cardiaco reveló un canal atrioventricular y atresia valvular pulmonar. El estudio ultrasonográfico abdominal mostró, en un corte subcostal longitudinal, un colector de 1 cm de diámetro que descendía por delante de la aorta abdominal y desembocaba en la vena porta (Figura 1). La angiotomografía reveló que el hígado estaba en posición horizontal y el estómago se ubicaba a la derecha de la línea media. Las venas pulmonares confluían en un colector que descendía a la derecha de la línea media, atravesaba el diafragma y se introducía al hígado para unirse a la vena porta (Figura 2). Ambos pulmones eran trilobulados y carecía de bazo (anesplenia).

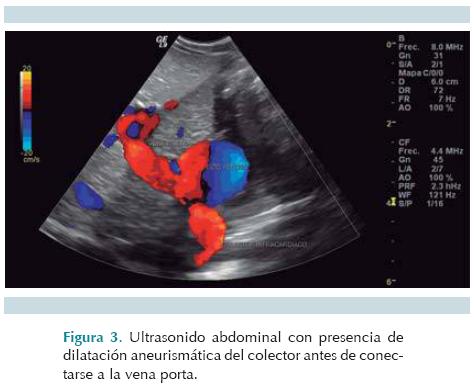
Caso 2. Niña de 6 meses de edad, nacida por parto normal; peso 3,400 g, APGAR 7-8. Al llegar al Instituto Nacioanl de Pediatría se la encontró con pobre esfuerzo respiratorio y cianosis; con saturación arterial de oxígeno entre 68 y 74%. Frecuencia cardiaca de 140 latidos por minuto y respiratoria de 45 por minuto. El ecocardiograma mostró yuxtaposición aortocava, comunicación interauricular tipo ostium primum, canal aurículo ventricular, con ventrículo derecho dominante; insuficiencia valvular AV, atresia de la válvula pulmonar; ramas arteriales pulmonares confluentes, conexión venosa pulmonar anómala, quizá mixta. Un corte sagital ultrasonográfico a nivel de epigastrio y tomando como referencia la vena porta, mostró que recibía un colector infradiafragmático de 1 cm de diámetro, con una dilatación aneurismática en forma de rizo antes de conectar con la vena porta (Figura 3). También había dextroisomerismo pulmonar y anesplenia.
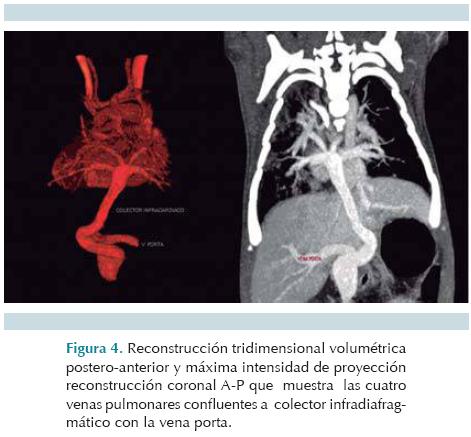
En las reconstrucciones tridimensionales volumétricas de la angiotomografía en proyección postero-anterior se observó la confluencia de las cuatro venas pulmonares a un colector infracardiaco largo, que se dirigía discretamente a la izquierda de la línea media, de aspecto tortuoso y una dilatación aneurismática antes de conectar con la vena porta (Figura 4).
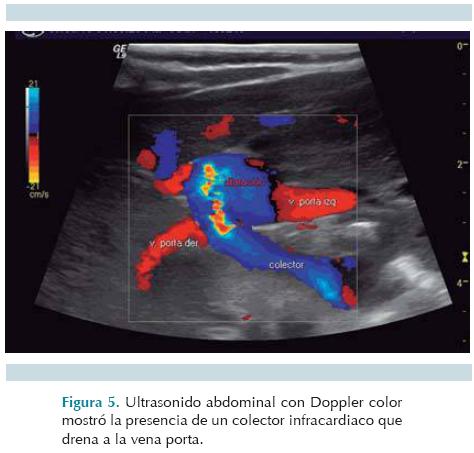
Caso 3. Niña de 58 días de edad, nacida del primer embarazo. Se realizaron 6 ultrasonidos prenatales; 4 se informaron normales; los dos últimos con oligohidramnios. Nació por parto a las 38 semanas de gestación con peso de 2,600 g. Se desconocen datos de APGAR y Silverman. Al parecer lloró y respiró al nacer sin necesidad de maniobras de reanimación. Salió del hospital a las 24 horas, durante una semana tuvo cianosis central y disnea a la alimentación. Fue valorada por los médicos del servicio de Cardiología del Instituto Nacional de Pediatría. El ecocardiograma mostró persistencia de conducto arterial, situs solitus, canal AV, probable drenaje anómalo de venas pulmonares y estenosis valvular pulmonar acentuada. El ultrasonido Doppler color (Figura 5) mostró un colector que conectaba a la vena porta, dato que se corroboró en las reconstrucciones coronales y tridimensionales volumétricas de la tomografía multicorte; también tenía dextroisomerismo pulmonar y ausencia de bazo (Figura 6).

Análisis
En la conexión anómala total de las venas pulmonares, la aurícula derecha recibe la sangre de ambas venas cavas y la sangre oxigenada de las cuatro venas pulmonares. Las manifestaciones clínicas de esta cardiopatía dependen de: 1) Presencia o no de una obstrucción del colector y 2) tamaño de la comunicación interauricular, sea un foramen oval, amplio o estrecho, ostium primum, ostium secumdum o canal AV persistente.
Los síntomas pueden aparecer horas después del nacimiento o días o semanas más tarde. Esto depende del sitio y la magnitud de la obstrucción que exista en el colector; datos relacionados con hiperflujo pulmonar, como: disnea, taquipnea, dificultad respiratoria y fatiga durante la alimentación. Puede haber algún grado de cianosis. La mayoría de los pacientes tiene síntomas en la primera semana de vida. Mientras el conducto arterial permanezca abierto, predominará la cianosis sobre la congestión pulmonar debido a que la presión pulmonar no será más alta que la presión sistémica, que retardaría la aparición de síntomas durante varias semanas.5
Los pacientes pueden agravarse rápidamente, con aumento de la cianosis y aparición de acidosis metabólica; aún cuando si no son extremas, la situación clínica puede permanecer estable durante días, pero se agrava bruscamente cuando se cierra el conducto arterial. En este caso la cianosis puede disminuir, pero aumenta la insuficiencia respiratoria; aparecen taquipnea y tiro intercostal, hepatomegalia y pulsos débiles. Los pacientes se ven levemente cianóticos y malnutridos. Existe abombamiento del precordio, con un impulso marcado del ventrículo derecho. En el segundo espacio intercostal izquierdo, sobre el borde esternal, puede escucharse un soplo sistólico eyectivo grado 2/4; el segundo ruido pulmonar se escucha acentuado y constantemente desdoblado. La radiografía de tórax muestra congestión de la vasculatura pulmonar, sobre todo a nivel de los hilios; los campos pulmonares se observan "velados" a causa del edema. La silueta cardiaca se ve aumentada de tamaño.1-6
Cuando el colector es largo y tiene una obstrucción como sucede en los drenajes a la vena porta se eleva la presión pulmonar y se reduce la saturación de oxígeno considerablemente porque en tal caso disminuye el flujo pulmonar y se eleva la presión venocapilar que conduce al edema pulmonar. Si el colector no tiene obstrucción, la saturación arterial puede estar entre 90 y 92% en vista de que la aurícula derecha sólo recibe 3 de 5 partes de sangre saturada proveniente de las venas pulmonares y pasa al ventrículo derecho y a la arteria pulmonar; esto sobrecarga las cavidades cardiacas derechas y causa hiperflujo pulmonar y origina insuficiencia cardiaca derecha.1,6,7
El 80-90% de los pacientes fallecen antes del primer año de vida si no se les trata quirúrgicamente, o mueren en los primeros meses de edad si existe una obstrucción del colector.3-6
En la conexión anómala total de las venas pulmonares infracardiacas el sitio de desembocadura anómala más frecuente es la vena porta. Son muy raros los casos informados con desembocadura en el ducto venoso, en las venas hepáticas en la vena cava inferior, en la vena esplénica o en la vena mesentérica superior. En ese tipo de conexión anómala la obstrucción del colector puede ser anatómica o funcional. La de tipo anatómico puede ser extrínseca (hiato esofágico) o intrínseca por estrechez del colector. La obstrucción funcional se debe a la resistencia del flujo sanguíneo intrahepático, que se interpone entre el sitio de la conexión a la vena porta y la entrada de sangre al corazón.2-6-7
El diagnóstico de esta cardiopatía se realiza, inicialmente, por ecocardiografía (estudio muy sensible para la evaluación morfológica y la funcional cardiaca). Sus principales limitaciones son: 1) La experiencia y habilidad del ecocardiografista. 2) La coexistencia de ventanas acústicas no siempre adecuadas. 3) La dificultad para evaluar en forma satisfactoria las estructuras extracardíacas, el sitio del drenaje del colector infracardiaco y las malformaciones broncopulmonares asociadas.
El cateterismo cardiaco permite evaluar las estructuras vasculares intra y extra cardiacas, y sus aspectos funcionales; sin embargo, es un estudio invasivo y prolongado. Hay que tener en cuenta que estos pacientes casi siempre se encuentran hemodinámicamente inestables al momento del estudio.
En la actualidad, con los tomógrafos helicoidales multicorte pueden visualizarse las estructuras vasculares, las del corazón y las extracardiacas en corto tiempo en fases arterial y venosa. El Cuadro 2 muestra la contribución y las limitaciones de los diferentes métodos de diagnóstico.
Importancia del ducto venoso
Durante la vida fetal, 50% del flujo sanguíneo umbilical pasa a la circulación capilar hepática a través del ducto venoso. Después del nacimiento, el flujo sanguíneo umbilical se suspende y el flujo sanguíneo pulmonar se incrementa. Mientras el ducto venoso siga permeable, el flujo venoso pulmonar que pasa por el vaso colector hacia la vena porta, puede ingresar directamente a la vena cava inferior y, por lo tanto, no causa hipertensión venosa pulmonar ni edema pulmonar.
La oclusión ducto venoso da por resultado que la sangre venosa pulmonar pase a través de la microcirculación hepática, esto eleva la presión de la vena porta y el drenaje venoso pulmonar, que es causa de edema pulmonar.
Cuando se cierra el ducto venoso, se dilata el sistema venoso portal y el flujo sanguíneo se retarda en la vena descendente, debido a la resistencia al flujo a través de los canales venosos largos y estrechos. Si el ducto venoso no es permeable, la conexión con la vena porta se obstruye, pues la circulación por el parénquima hepático enfrenta una resistencia elevada. Si la vena descendente conecta con la vena cava inferior o con la vena hepática y no hay datos clínicos ni ecocardiográficos de obstrucción, el paciente puede operarse con menos premura que cuando conecta con el ducto venoso o el sistema venoso portal.6,7,10
Nuestras pacientes fallecieron quizá debido a obstrucción del colector y a edema pulmonar.
La corrección quirúrgica consiste en ligar la vena descendente lo más distalmente posible (puede o no seccionarse), siguiendo la dirección de su mayor tributaria. Enseguida se incide la pared posterior de la aurícula izquierda, paralelamente a la confluencia venosa pulmonar y se anastomosa de manera latero lateral.6-11
La mortalidad quirúrgica de pacientes operados por expertos varía entre 2 y 20%. Esto se debe a la gravedad de la malformación, a la corta edad de los enfermos, a su bajo peso y a la rareza de la cardiopatía. La supervivencia a largo plazo depende, en buena medida, de una intervención bien ejecutada. La muerte en los primeros meses postoperatorios es infrecuente; casi siempre se debe a estenosis de las venas pulmonares.1-6,12,13
Entre 5 y 10% de los operados resultan con estenosis de la anastomosis, con alto grado de mortalidad meses o años después del procedimiento quirúrgico.
CONCLUSIONES
El estudio de esta afección se ha efectuado con angiografía convencional y cateterismo cardiaco; este último ha permitido diagnosticar malformaciones asociadas.
La tomografía computada helicoidal multicorte, con acceso a estaciones de procesamiento gráfico, obtiene imágenes tridimensionales volumétricas que revelan anomalías congénitas complejas con gran precisión. En nuestras tres pacientes se corroboró el canal aurículo-ventricular y dextroisomerismo.14
Las ventajas de la tomografía son que el estudio se realiza en un tiempo corto, de 15 a 20 segundos (apnea inspiratoria); los tomógrafos multicorte de 320 detectores o los equipos duales son aún más rápidos; se obtienen, entre otras, imágenes angiográficas en fases arterial y venosa, que pueden evaluarse en diferentes planos; se obtiene información de estructuras adyacentes como: pulmón, la porción inferior del cuello y superior del abdomen, todo ello con una sola inyección de 1-2 mL/kg de peso de medio de contraste. Las limitaciones de la tomografía multicorte son: la radiación, aunque en menor dosis que en estudios angiográficos, la anestesia, y el uso de medio de contraste (cantidades mínimas). Son muy raros los casos de alergia a los medios de contraste hidrosoluble.15
La interpretación de los estudios debe hacerse por radiólogos pediatras experimentados en este tipo de anormalidades, como se hizo en nuestros pacientes.
Agradecimiento a: Dr. Jorge Espino Vela por sus valiosas observaciones para este trabajo.
REFERENCIAS
1. Espino Vela J. Cardiologia Pediátrica. 3a Ed. México: Méndez Editores, 1994; capítulo 13. [ Links ]
2. Muñoz-Castellanos L, Sánchez C. Conexión anómala de venas pulmonares. Correlación anatomoembriológica. Arch Cardiol México 2008;78:247-54. [ Links ]
3. Garson A, Bicker T. The science and practice of pediatric cardiology. Vol 2. New York: Lea & Febiger, 1990;1145-74. [ Links ]
4. Manzo-Ríos MA, Anaya-García JE. Conexión anómala de venas pulmonares infracardiaca. Bol Clin Hosp Infant Edo Son 2007;24:424. [ Links ]
5. Burroughs JT, Edwards JE. Total anomalous pulmonary venous connection. Am Heart J 1956;31:182. [ Links ]
6. Attié F, Zabal C, Buendía A. Cardiología Pediátrica. 1ª ed. México:Médica Panamericana 2009;38-50. [ Links ]
7. Rudolph AM. Congenital diseases of the heart. Clinical-physiological considerations. Chapters 11 and 13. Atlanta: Futura Publishing, 2001. [ Links ]
8. Gersony WM. Presentation, diagnosis and natural history of total anomalous pulmonary venous drainage. In: Godman MJ, Marquis RM (eds). Paediatric Cardiology, Heart Disease in the Newborn. Vol .2. London: Churchill Livingstone, 1997;163. [ Links ]
9. Gersony WM, Bowman FO, Steeg CN, Hayes CJ, Jese MJ, Malm JR. Management of total anomalous pulmonary venous drainage in early infancy. Circulation 1971;(Suppl I):119. [ Links ]
10. Telles G. Tratado de Cirugía Cardiovascular. México: Ediciones Santos, 2000;150-156. [ Links ]
11. Gathman GE, Nadas AS. Total anomalous pulmonary venous connection: clinical and physiologic observations of 75 pediatric patients. Circulation 1970;42:143. [ Links ]
12. Edwars JE. Pathologic and developmental consideration in anomalous pulmonary venous connection. Proc Staff Meet Mayo Clin 1953;28:441-52. [ Links ]
13. Castañeda AR, Jonas RA, Mayer JE, Hanley FL. Anomalies of pulmonary veins. In: Cardiac Surgery of Neonates and Infant. Philadelphia: WB Saunders, 1994;157-66. [ Links ]
14. Kimberly E, Marilyn J, Gregory Pierce. Situs revisted: imaging of hetrotaxy Syndrome. Radiographics 1999;19:837-852. [ Links ]
15. Himesh V, Vays S, Greenberg B. MR imaging and CT Evaluation of Congenital Pulmonary Vein Abnormalities in neonates and infants. Radiographics 2012;32:87-98. [ Links ]
Nota
Este artículo debe citarse como
Solórzano-Morales SA, López-ElÃas FJ, López-Terrazas JH, Bernal-Moreno M, Palacios-Macedo-Quenot AJ, Bobadilla-Aguirre A. Conexión anómala total de venas pulmonares a la vena porta. Valor de la angiotomografía multicorte. Informe de tres casos. Acta Pediat Mex 2014;35:22-29.














