Introducción
Durante años el oxígeno suplementario ha sido administrado a través de diferentes dispositivos (puntas nasales y mascarillas) al ser la primera línea de tratamiento para falla respiratoria hipoxémica. El oxígeno que proveen estos sistemas tiene diversas limitaciones que no causan consecuencias clínicas en la mayoría de las circunstancias debido a que la entrega de flujo de oxígeno es suficiente para corregir la hipoxemia.
Algunos inconvenientes descritos son la poca tolerancia por humidificación, el flujo frío de oxígeno y una entrega no mayor de 15 L/min de oxígeno. Estos dispositivos muestran una diferencia entre el flujo de oxígeno y la cantidad del mismo a la inspiración, variando entre 30 y 120 L/min durante falla respiratoria.
La proporción inspirada de gas humidificado y oxigenado puede ser muy pequeña (menos de 10%), dependiendo de la extensión de oxígeno diluido en el aire ambiental. Una consecuencia directa es que la fracción inspirada de oxígeno no es constante durante la terapia de oxígeno convencional y, por lo tanto, es aproximada. La entrega de oxígeno depende de la vía aérea del individuo; su permeabilidad debe ser evaluada antes de iniciar el apoyo de oxígeno.
La concentración de oxígeno debe ser titulada para un objetivo de saturación, que debe ser entre 94-98% para la mayoría de los sujetos, u 88-92% para aquéllos con falla respiratoria hipercapnia a nivel del mar.
Las indicaciones de oxigenoterapia son:
Hipoxemia aguda.
Isquemia asociada a hipoxemia.
Anormalidades en la cantidad, calidad o tipo de hemoglobina.
Neumotórax.
Estado perioperatorio.
Disminución de la concentración de oxígeno.
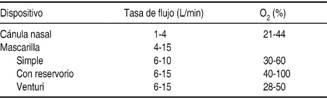
Selección de equipos. Hay dos tipos de dispositivos de entrega de oxígeno: los de funcionamiento variable o los de funcionamiento fijo. Los dispositivos de funcionamiento variable como la mascarilla facial/tienda de traqueostomía (sin dispositivo Venturi) o cánula nasal no pueden otorgar un porcentaje de FiO2 fijo, ya que es dependiente de la frecuencia respiratoria y el volumen tidal. Los dispositivos de funcionamiento fijo intentan entregar un porcentaje de oxígeno independientemente de la frecuencia respiratoria de la persona o el volumen tidal.
Los diferentes dispositivos de entrega de oxígeno se pueden ver en el Cuadro I.
La ventilación mecánica no invasiva (VMNI) se define como el ingreso de aire a los pulmones con máquinas que generan una presión positiva, pero mantienen la vía aérea libre de tubo endotraqueal.1,2
Se requieren interfases, que son dispositivos que se colocan al final del circuito del ventilador y están en contacto con el enfermo. Existen varios tipos de interfases: nasal, facial, frontomentoniana y casco. La utilidad de ellas depende de la comodidad con el paciente, el espacio muerto reducido y el impedimento de las fugas.3
Las modalidades de ventilación mecánica no invasiva (VMNI) en un individuo son el resultado de tres variables: el control de inicio de la inspiración, el control de la inspiración-espiración y las características de la onda de flujo y presión producidos por el ventilador. Existen varios modos ventilatorios, los limitados por presión, volumen, presión soporte y CPAP (Continuous positive airway pressure).4,5
Algunos de los efectos fisiológicos de la VMNI surgen tras la aplicación de una presión positiva supraatmosférica en la vía aérea originando un gradiente de presión que da lugar al flujo inspiratorio por lo que se realiza la espiración de forma pasiva debido a la retracción elástica pulmonar. Para un determinado gradiente de presión, el flujo generado dependerá de la resistencia de las vías aéreas; por otra parte, el cambio de volumen alveolar, secundario a dicho flujo de aire, dependerá de la elastancia o resistencia elástica del pulmón; aumenta la ventilación en las zonas de espacio muerto e hipoventila las zonas más perfundidas debido a las diferencias en la distensibilidad alveolar.
En sujetos con falla respiratoria aguda y crónica, consigue una ventilación suficiente para mantener un intercambio gaseoso adecuado, corrigiendo la hipoventilación alveolar, disminuyendo el trabajo ventilatorio y mejorando la función de los músculos respiratorios.
Los niveles de evidencia para uso de VMNI en falla respiratoria aguda son:
En personas seleccionadas apropiadamente con falla respiratoria hipoxémica (Nivel I).
En pacientes de UCI con falla respiratoria aguda hipoxémica (Nivel II).
En síndrome de insuficiencia respiratoria aguda (SIRA) puede ser usada con gran precaución en casos de lesión pulmonar aguda y sólo UCI (Nivel III). Se reserva para individuos hemodinámicamente estables.
Existen actualmente dispositivos de alto flujo que son usados en la práctica clínica para entregar oxígeno a una velocidad de flujo que supera la velocidad de flujo normal del sujeto, siendo capaces de entregar de manera más precisa una fracción inspirada de oxígeno (FiO2).6 El sistema básicamente funciona con un mezclador de aire de oxígeno, permitiendo tener una FiO2 desde 21 al 100% y generando flujos hasta de 60 L/min. El entregar altos niveles de oxígeno puede ocasionar sequedad en la vía aérea, condicionando disconformidad. Para mejorar el confort y la eficacia, las puntas nasales de alto flujo otorgan oxígeno caliente y humidificado. El gas es calentado y humidificado activamente; posteriormente, se entrega por un circuito de calentamiento inspiratorio de una sola rama (para evitar pérdida de calor y condensación) hacia la persona a través de cánulas nasales de un diámetro amplio. Las puntas nasales de alto flujo proveen bajo nivel de presión positiva de la vía aérea, reducen su resistencia y disminuyen el espacio muerto nasofaríngeo; proporcionan una pequeña y variable cantidad de presión positiva al final de la espiración (PEEP: positive end-expiratory pressure) de 1 cmH2O por cada 10 L/min de flujo. Existe una relación entre flujo y presión, donde se observa una relación positiva lineal entre el flujo con una presión positiva de la vía aérea de 2.7 cm H2O a 35 L/min.7-9 Un efecto principal ante la entrega de oxígeno a alto flujo directamente a la nasofaringe es el lavado de CO2 y la reducción de su reinhalación, proporcionando un reservorio de gas fresco con disminución del espacio muerto y aumento de la ventilación alveolar en relación de un minuto. Estas propiedades tienen beneficios clínicos en tolerancia al ejercicio, reducción de disnea y mejor oxigenación.10 El diseño de la nasofaringe facilita la humidificación y calentamiento del gas inspirado al contacto con una larga área de superficie; al ser esta superficie húmeda, puede producir una resistencia al flujo de gas de manera apreciable.11
Material y métodos
Objetivo del trabajo: el objetivo es dar respuesta a la pregunta PICO «si en población con diagnóstico de SIRA leve, las puntas nasales de alto flujo disminuyen la intubación orotraqueal comparadas con el uso de VMNI».
Para dar una respuesta a la pregunta PICO, se hizo una búsqueda exhaustiva en las siguientes bases de datos:
Registro Cochrane Central de Ensayos Controlados (CENTRAL) en The Cochrane Library; MEDLINE, OvidSP (todos los artículos); EMBASE (todos los artículos); ISI Web of Science (todos los artículos); PubMed (todos los artículos). Sólo se incluyeron estudios en el idioma inglés, utilizando palabras MeSH como «acute hypoxemic respiratory failure», «acute respiratory failure», «acute lung injury», «acute respiratory distress syndrome», «acute respiratory distress syndrome (ARDS)», «respiratory distress syndrome, acute», «respiratory distress syndrome, adult», «ARDS, human», «high-flow nasal», «nasal», «high-flow», «oxygen», «therapy», «noninvasive ventilation». Se tuvo como resultado 14 artículos relevantes. La fecha de búsqueda se restringió a 20 años; como no existen estudios que analicen VMNI versus HNFC, también se buscaron artículos que hablaran de HNF, VMNI en insuficiencia respiratoria aguda en adultos.
Búsqueda de otros recursos: se examinaron las listas de referencias de los ensayos elegibles para identificar cualquier estudio no ubicado previamente, así como las bibliografías de los estudios encontrados para revisar si algún estudio no se incluyó.
Medidas del efecto del tratamiento: se intentó realizar el análisis estadístico mediante Review Manager 5 (RevMan 5.1). Debido a la poca evidencia de estudios que existen a la fecha, se realizó una revisión detallada de toda la bibliografía existente en adultos sobre HNF, VMNI e insuficiencia respiratoria. Se elaboró una tabla donde se resumen los estudios.
Resultados
Se encontraron 14 artículos después de la revisión de la literatura publicada. Se analizó cada uno de ellos, excluyéndose los artículos de revisión, los casos clínicos o los de población pediátrica. Quedaron únicamente tres artículos (Cuadro II).
Discusión
En la revisión se pide hablar de SIRA leve; sin embargo, la definición de Berlín15 en 2012 hace que exista un parteaguas en cuanto a criterios; por lo tanto, antes de 2012 se tienen estudios con poblaciones heterogéneas, donde se menciona «insuficiencia respiratoria aguda», sin alguna otra clasificación. En los últimos años, las puntas de alto flujo han tenido gran impacto, pues han demostrado su utilidad en la insuficiencia respiratoria hipoxémica debido a su presión positiva generada al final de la espiración, como lo demostró Groves en 2007.8 Éste es un estudio de alta referencia bibliográfica para la literatura pública posteriormente, haciendo mención a la presión positiva final que se genera; sin embargo, los participantes fueron voluntarios sanos y de una muestra no representativa sin grupo control (cinco pacientes). Parke,16 en 2009, realizó un estudio en población postquirúrgica para demostrar el efecto de la presión positiva al final de la espiración (PEEP); su grupo control fue la misma población pero en diferente momento, el dispositivo a comparar fue la mascarilla facial (el cual no es un dispositivo que proporcione presión positiva) y el flujo máximo de las puntas nasales de alto flujo fue de 35 L/min. Concluyó que se obtenía una presión positiva mayor comparada con la mascarilla facial y este efecto era mayor si era con la boca cerrada; la muestra fue sin alteraciones respiratorias y un grupo no significativo; no se mencionan comorbilidades que hubieran tenido los individuos.
Se habla del beneficio del lavado de CO2 al proporcionar flujos altos, existiendo casos clínicos donde se demuestra esto,17 sin embargo, Roca y colaboradores18 demostraron que no existe diferencia en la PaCO2 entre puntas nasales de alto flujo y la mascarilla Venturi; aunque su estudio fue con sujetos con SIRA, su objetivo primario fue comparar la comodidad de la terapia de oxígeno a través de la terapia de alto flujo versus mascarilla Venturi, asociándose con menos disnea, sequedad bucal y mayor confort; todas estas variables con significancia estadística. En 2011, Parke19 realizó un estudio con el objetivo de comparar las puntas nasales de alto flujo versus mascarilla Venturi en personas con hipoxemia moderada; sin embargo, su resultado fue tolerancia, la cual no menciona cómo evaluó. Rello20 llevó a cabo un trabajo donde su objetivo fue la necesidad de valorar VMNI y mortalidad con el uso de PAF, así como identificar qué enfermos se benefician más de dicha terapia. Fue un estudio retrospectivo de un análisis post hoc de una cohorte de pacientes ingresados por influenza; no existió una comparación como tal entre dos grupos, solamente comparó un grupo de individuos que recibió oxigenoterapia de manera habitual contra un grupo que falló a esa oxigenoterapia y al que le fue colocado HNF. Los grupos no fueron aleatorizados; en el grupo de no respondedores, se encontró que a las seis horas los sujetos con falla a las HNF tenían una PaO2/FiO2 significativamente más baja de 73 versus 135. En este estudio se concluyó, además, que las personas con enfermedad pulmonar obstructiva crónica (EPOC) son quienes mejor toleran las puntas nasales. Stéphan,21 en 2014, en una población específica de enfermos postquirúrgicos cardiacos, encontró que las puntas de alto flujo eran superiores a la ventilación no invasiva, pero el criterio de inclusión fue que los pacientes hubieran fallado a la prueba de respiración espontánea, además de que en el grupo con VMNI fue un tratamiento que no fue constante durante su aleatorización.22
Conclusión
Actualmente no existe evidencia suficiente de buena calidad metodológica para hacer una recomendación en el uso de las puntas nasales de alto flujo en SIRA leve; hacen falta más estudios aleatorizados que comparen puntas de alto flujo versus ventilación mecánica no invasiva en individuos bajo la definición universal actual de SIRA.











 nueva página del texto (beta)
nueva página del texto (beta)