Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista mexicana de ciencias farmacéuticas
versión impresa ISSN 1870-0195
Rev. mex. cienc. farm vol.45 no.3 Ciudad de México jul./sep. 2014
Revisión bibliográfica
Principales sistemas osmóticos orales
Main oral osmotic systems
José Eduardo Hernández Torres1 y Luz María Melgoza Contreras2
1 Maestría en Ciencias Farmacéuticas, Universidad Autónoma Metropolitana, Unidad Xochimilco, México.
2 Departamento de Sistemas Biológicos, Universidad Autónoma Metropolitana, Unidad Xochimilco, México.
Correspondencia:
Dra. Luz María Melgoza Contreras
Departamento de Sistemas Biológicos
Universidad Autónoma Metropolitana, Unidad Xochimilco
Calzada del Hueso 1100 Col. Villa Quietud Delegación
Coyoacán C.P. 04960, México D.F., México
Tel: 54-83-70-00 Ext: 3629
Correo electrónico: lmelgoza@correo.xoc.uam.mx
Fecha de recepción: 29 de octubre de 2013
Fecha de recepción de modificaciones: 20 de julio de 2014
Fecha de aceptación: 30 de septiembre de 2014
Resumen
Los sistemas de liberación convencionales tienen poco control sobre la liberación del fármaco, lo que resulta en concentraciones plasmáticas variables. Como consecuencia, se han desarrollado sistemas de liberación controlada, como los sistemas osmóticos que han demostrado ser independientes de las condiciones fisiológicas del cuerpo (pH, alimento y movimientos peristálticos). La liberación del fármaco puede controlarse conociendo de antemano las propiedades fisicoquímicas del fármaco y la forma de dosificación. Esta revisión señala los conceptos teóricos de la liberación del fármaco en estos sistemas, incluyendo sus ventajas y desventajas; los diferentes tipos de sistemas osmóticos orales, los factores que afectan a estos sistemas, así como su situación en el mercado.
Palabras clave: Liberación controlada, vía oral, ósmosis, presión osmótica, membrana semipermeable.
Abstract
The conventional delivery systems have a poor control over drug released, resulting in variable plasmatic levels. As a result, systems of osmotic controlled release have been developed; they are independent of body's physiological conditions (pH, food and peristalsis). Drug release can be programmed by knowing physicochemical properties of the drug and the dosage form. This review discusses: theoretical concepts of drug releasing in these systems, including their advantages and disadvantages; different kinds of oral osmotic systems, also the factors affecting these systems and their status in the market.
Keywords: Controlled release, oral via, osmosis, osmotic pressure, semipermeable membrane.
Introducción
En un régimen terapéutico típico, la dosis del fármaco y el intervalo de dosificación están optimizados para mantener la concentración de fármaco dentro de la ventana terapéutica, garantizando así la eficacia mientras minimiza los efectos tóxicos.1
En los sistemas de administración orales convencionales a menudo se presenta una concentración ineficaz del fármaco en el sitio de acción, a consecuencia de ello este tipo de dosificación resulta impredecible, presentándose efectos secundarios. Una liberación rápida y descontrolada del fármaco podría resultar en una toxicidad sistémica o local. Más aún, la velocidad y el grado de absorción del fármaco en este tipo de formulaciones puede variar enormemente, dependiendo de factores fisicoquímicos del fármaco, excipientes que lo acompañan o factores fisiológicos.2
Las tecnologías avanzadas en la liberación de fármacos pueden mejorar dichos productos, tanto en cuestiones intrínsecas como son, la eficacia y control del mismo así como extrínsecas, ya sea por su valor comercial o como un recurso eficaz de competencia mercantil.3
Los sistemas de liberación controlada proporcionan una concentración uniforme de fármaco en el sitio de absorción, por lo tanto, después de la absorción permiten el mantenimiento de las concentraciones plasmáticas dentro de un intervalo terapéutico, lo que minimiza los efectos secundarios y también reduce la frecuencia de administración.2
Los sistemas osmóticos poseen un diseño adecuado para la liberación controlada de fármacos, los cuales se basan en el principio de la presión osmótica. Estos sistemas no se ven influenciados por los diferentes factores fisiológicos existentes, así también presentan una liberación de fármaco predecible a partir de las propiedades conocidas del fármaco y de la forma de dosificación, modulando las propiedades del mismo sistema.1,3
El presente trabajo revisará los principales sistemas osmóticos orales de liberación controlada más utilizados, englobando su diseño, funcionamiento y aspectos basados en su formulación.
Desarrollo histórico
El inicio de esta tecnología se presentó cuando Rose y Nelson en 1955 utilizaron el principio de presión osmótica en la liberación de fármacos. El dispositivo que desarrollaron consistía de tres cámaras: una de fármaco, otra contenía sal en exceso y por último una cámara de agua. El dispositivo contaba con un diafragma de látex que separaba la cámara de sal con la de fármaco; también contaba con una cámara semipermeable que separaba las cámaras de agua y de sal. La diferencia en la presión osmótica entre estas dos cámaras movía el agua desde la cámara de agua hasta la cámara de sal a través de la membrana. El volumen de la cámara de sal al mismo tiempo se incrementaba formando un flujo de agua, distendiendo el diafragma de látex, liberando el fármaco al exterior del dispositivo.4 Sin embargo el uso de estos dispositivos fue limitado, pues debido a su complejidad en cuanto al diseño, se dificultó su producción a gran escala.
Para los años 70's, Higuchi y Leeper propusieron una serie de variaciones de la bomba de Rose y Nelson,5,6,7 y por otro lado Theeuwes continuó realizando modificaciones hasta diseñar la bomba osmótica elemental (BOE).8,9,10 Esto último dio pie a una serie de patentes, provenientes la mayor parte de la firma Alza Corporation (aproximadamente un 90% de las patentes existentes son de su propiedad) para diferentes sistemas de liberación y vías de administración, que recurren a la presión osmótica como fuente impulsora.2 Sin embargo, muchas de estas patentes han expirado y otras están próximas a hacerlo, lo que ha incrementado el interés en el desarrollo de bombas osmóticas para liberación controlada.
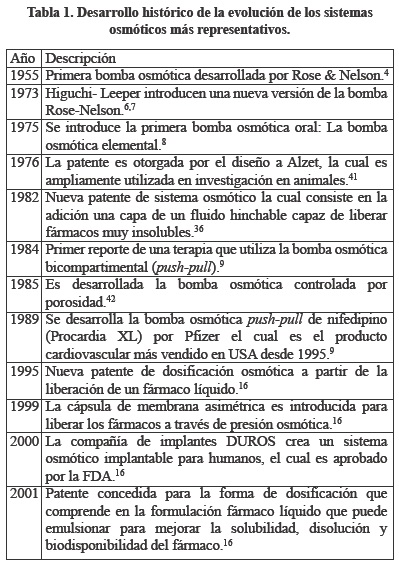
Con el paso del tiempo se han desarrollado diversos dispositivos, así como modificaciones, que actúan a partir de la presión osmótica. En la tabla 1 se presentan los primeros dispositivos osmóticos y los avances más significativos de estos sistemas hasta la actualidad.
Ventajas y desventajas de los sistemas osmóticos1,2,3,11,12,13,14
Los sistemas osmóticos para uso oral ofrecen distintas ventajas sobre otros medios de entrega de fármacos y son:
1. La liberación del fármaco es independiente del pH gástrico y la presión hidrodinámica del intestino.
2. La liberación de los sistemas osmóticos no se ve afectada por la presencia de alimentos en el tracto gastrointestinal.
3. Suelen dar un perfil de liberación de orden cero después de un tiempo lag inicial.
4. Están caracterizados sus mecanismos de acción.
5. Los mecanismos de liberación no son dependientes del fármaco.
6. Estos sistemas permiten formular medicamentos con fármacos de diversas solubilidades.
7. La velocidad de liberación de los sistemas osmóticos es altamente predecible y se puede programar mediante la modulación de los parámetros de control de la liberación.
8. Poseen un alto grado de correlación in vitro e in vivo.
Entre las principales limitaciones propias de este tipo de sistemas encontramos que son formulaciones costosas, sumando que si el proceso de recubrimiento no está bien controlado existe el riesgo de defectos en la membrana, lo que resulta en una velocidad de liberación impredecible, vaciado de la dosis y aparición de efectos secundarios.1,2,3,14
Shapiro y col. (1996) en un estudio señalan que durante el control de calidad aplicado a tabletas de nifedipino, algunos lotes mostraban diferentes patrones de liberación del fármaco. Usando imágenes obtenidas por resonancia magnética nuclear, se encontró que el recubrimiento pelicular alrededor de la tableta producía diferentes espesores de membrana, lo cual fue la causa principal de los diferentes patrones de velocidad de liberación entre los diferentes lotes.15
A pesar de la aparición de este tipo de casos, los sistemas de liberación osmótica han mostrado beneficios clínicos significativos gracias a que han potenciado la eficacia del fármaco y minimizado efectos adversos de algunos principios activos, por lo que se ha incrementado su uso.
Bomba osmótica elemental (BOE)
Este dispositivo fue inventado por Theeuwes en 1974 conocido como OROS® (Osmotic Release Oral System) el cual contiene esencialmente un agente osmótico que brinda una presión osmótica adecuada, asimismo se elabora como un comprimido recubierto por una membrana semipermeable, por lo general acetato de celulosa y se perfora un orificio en una de sus caras (Figura 1).8,11

Al momento en que el comprimido se expone a un ambiente acuoso, la presión osmótica del fármaco y del agente osmótico aumenta, debido al paso de agua a través de la membrana semipermeable formando una solución acuosa saturada de fármaco en el interior del dispositivo. La membrana no se extiende y a consecuencia se ejerce un aumento en el volumen debido a la captación de agua lo que produce presión hidrostática en el interior de la tableta, llevando eventualmente la solución saturada del fármaco fuera del dispositivo a través del orificio realizado. Esto se puede representar en la ecuación (1).

Donde  es la velocidad de entrada del agua, A y h son el área y el espesor de la membrana, respectivamente, Lp es la permeabilidad mecánica de la membrana, σ es el factor de semipermeabilidad, Δπ y Δp son las diferencias de presión osmótica e hidrostática, respectivamente y C es la concentración de fármaco en solución. La ecuación anterior puede simplificarse, considerando un orificio que permita despreciar la presión hidrostática dentro del sistema y ejerciendo una presión osmótica en el núcleo mucho mayor que la externa (Δπ>Δp), por tanto reemplazando Lp, p y σ por K considerándose como la constante de la permeabilidad de la membrana, obteniendo la ecuación (2).
es la velocidad de entrada del agua, A y h son el área y el espesor de la membrana, respectivamente, Lp es la permeabilidad mecánica de la membrana, σ es el factor de semipermeabilidad, Δπ y Δp son las diferencias de presión osmótica e hidrostática, respectivamente y C es la concentración de fármaco en solución. La ecuación anterior puede simplificarse, considerando un orificio que permita despreciar la presión hidrostática dentro del sistema y ejerciendo una presión osmótica en el núcleo mucho mayor que la externa (Δπ>Δp), por tanto reemplazando Lp, p y σ por K considerándose como la constante de la permeabilidad de la membrana, obteniendo la ecuación (2).

La velocidad de liberación definida por la ecuación anterior es de orden cero siempre y cuando los términos de la ecuación se mantengan constantes. Por lo tanto, para obtener una liberación de fármaco constante esta dependerá de la correcta selección de la membrana y de la formación de una solución saturada del fármaco dentro del núcleo que permita obtener una concentración en solución constante.1,2,3,8,16
Factores que afectan la liberación del fármaco
Solubilidad
La cinética de liberación del fármaco en un sistema osmótico está directamente relacionada con su solubilidad en agua para la formación de la solución saturada correspondiente dentro del núcleo. Si se asume que este último está constituido por fármaco puro, es posible calcular la fracción de fármaco liberado (Ecuación 3) con cinética de orden cero (F(z)).

Donde S es la solubilidad del fármaco (g/mL) y p es la densidad del núcleo de la tableta (g/mL). De acuerdo con esta ecuación, los fármacos con una solubilidad menor de 0.05 g/mL deberían ser liberados en más de un 95% con cinética de orden cero, pero considerando la ecuación anteriormente explicada en la sección de BOE, su velocidad de liberación sería muy baja debido al bajo gradiente osmótico que se generaría. Por el contrario, fármacos altamente solubles en agua serían liberados en baja proporción, siguiendo una cinética de orden cero y de acuerdo a la ecuación a una mayor velocidad de liberación.12,16 De ahí la importancia de considerar el valor de la solubilidad intrínseca del fármaco para buscar alternativas de formulación, como incluir ingredientes auxiliares que permitan modular su solubilidad en el núcleo. Tales alternativas, pueden ser la co-compresión del fármaco con otros excipientes16, el recubrimiento del núcleo con membranas asimétricas17,18, el uso de polímeros hinchables los cuales se hinchan después de absorber el agua y empujan el fármaco poco soluble en agua desde el orificio en forma de una suspensión finamente dividida9, derivados de ciclodextrinas,19 entre otros.16
Presión osmótica
La velocidad de liberación del fármaco en un sistema osmótico es directamente proporcional a la presión osmótica que se ejerce en el núcleo. Si la membrana semipermeable separa una solución de agua o dos soluciones diferentes con concentración de fármaco diferente existe una tendencia a equilibrar la concentración como resultado del flujo de agua. Es de importancia optimizar la presión osmótica entre el núcleo y el medio externo. La manera más simple y más predecible para conseguir una presión osmótica constante es mantener una solución saturada de agente osmótico en el compartimento o núcleo. Si una solución saturada del fármaco no posee suficiente presión osmótica, se debe agregar un agente osmótico adicional a la formulación del núcleo.1,2 Algunos de los compuestos osmóticamente activos más empleados se muestran en la tabla 2.

Tamaño de orificio
Los sistemas osmóticos contienen al menos un orificio en la membrana para la liberación del fármaco. El tamaño de orificio debe ser optimizado con el fin de controlar dicha liberación. El orificio no debe ser muy grande, puesto que permitiría la difusión del soluto a través de él. Asimismo el orificio no debe ser demasiado pequeño porque afectaría la liberación de orden cero y se desarrollaría un aumento en la presión hidrostática dentro del núcleo. Este aumento conllevaría a una deformación del dispositivo resultando en una liberación impredecible.2,11
Malaterre y col. (2008) hacen una comparación de tamaño de orificio que va de 0.5 mm hasta 1.5 mm, en los cuales confirman que en este intervalo de diámetro no se presentan variaciones en cuanto a la liberación del fármaco.20
Dichos orificios pueden ser realizados por medio de taladro mecánico, o rayos láser, las cuales son las técnicas más utilizadas. En algunos sistemas osmóticos, la perforación consiste en la incorporación de agentes formadores de poros, incorporados en la solución de recubrimiento. Estos agentes son solubles en agua y al contacto con el medio acuoso se disuelven creando poros.21
Membrana semipermeable
La liberación de los fármacos en los sistemas osmóticos es independiente del pH y la agitación del tracto gastrointestinal, por lo que la membrana es un aspecto muy importante en el control de la liberación del fármaco. Esto es debido a la selectividad de la membrana y a la efectiva aislación del proceso de disolución del ambiente intestinal. La membrana en los sistemas osmóticos, tiene que ser semipermeable, constituida principalmente por cualquier polímero que sea permeable al agua pero impermeable al soluto (fármaco, iones orgánicos e inorgánicos).2,8
Entre los principales polímeros utilizados para este fin están la etilcelulosa, copolímeros derivados de ácido metacrílico, ésteres de celulosa (acetato, triacetato, propionato y butirato de celulosa, entre otros) los cuales su permeabilidad dependerá de su grado de acetilación.22,23
En cuanto a los derivados de celulosa, éstos pueden incrementar su permeabilidad al agua con la adición de agentes plastificantes o de agentes hidrofílicos como los polietilenglicoles PEG 300, 400, 600, 1500, 4000 y 6000.2,24 La etilcelulosa pura tiene un uso limitado como membrana de recubrimiento de sistemas osmóticos, debido a su baja permeabilidad al agua, pero combinada con hidroxipropil metil celulosa(HPMC) mejora esta propiedad.25
Para asegurar que la membrana sea capaz de resistir la presión dentro del dispositivo, el espesor se recomienda estar en el intervalo de 200 a 300 µm.26 Sin embargo, esto puede ser un problema en los casos donde el fármaco posee una baja presión osmótica, lo cual conduce a una liberación lenta. En estos casos se recomiendan membranas altamente permeables.
Es importante resaltar que la velocidad de liberación de un sistema osmótico es inversamente proporcional al espesor de la membrana. Esto de acuerdo con la ecuación (1). Verma y col. (2002) reportaron que la liberación del fármaco en función del espesor de la membrana muestra que un incremento de dicho espesor en un intervalo de 9 a 50 µm, la liberación del fármaco disminuye.16 En el caso de tabletas osmóticas monolíticas de nifedipino, la liberación disminuyó al incrementar el espesor de 85 a 340 µm. Un incremento de la resistencia en la membrana ocurre cuando hay un mayor espesor, lo que provoca que la difusión del agua sea más lenta.27
Bombas osmóticas multicompartimentales
Bomba osmótica bicompartimental
Este sistema es conocido como push-pull OROS® consiste en un comprimido bicapa recubierto por una membrana semipermeable y una perforación en una de sus caras (Figura 2). La capa inferior o capa de empuje contiene un polímero hidrófilo (agente polimérico osmótico) capaz de formar un hidrogel expandible que empuja el compartimento superior o capa del fármaco. Este comprimido osmótico actúa mediante el efecto combinado de la hidratación de sus dos compartimentos de modo que, inicialmente la capa del fármaco absorbe agua suficiente para formar una suspensión o solución que será expulsada a través del orificio de salida tan pronto como se inicie la formación de un fluido en su interior y se dé la expansión y empuje por parte del compartimento inferior previamente hidratado.2,28,29

En el caso de los principios activos utilizados en este tipo de sistemas, se encuentran los principios activos muy solubles, en el cual el agua atraviesa la membrana semipermeable, disolviendo el principio activo, siendo expulsado a una velocidad dependiente de la presión osmótica del mismo principio activo y la expansión del hidrogel que va formando en la capa de empuje. Cuando el principio activo está disuelto completamente y la solución en la capa de empuje deja de ser saturada, el hidrogel continuará expandiéndose y compensará en cierta medida la perdida de presión osmótica en la capa del fármaco. En los principios activos poco solubles, la capa del fármaco debe de formularse de tal manera que se forme una suspensión al momento de la entrada de agua, lo más conveniente es que venga acompañado de agentes estabilizadores de suspensión.20,30,31
Los hidrogeles utilizados deben expandirse lo suficiente para expulsar la totalidad del fármaco contenido, sin producir ruptura en la membrana. Se utilizan regularmente polímeros hidrofílicos, formadores de hidrogeles en ambos compartimientos, en el caso de que la difusión del fármaco hacia la capa del fármaco y la interdifusión de ambos polímeros sean mínimas. Esto se consigue empleando polímeros con pesos moleculares diferentes, sean químicamente diferentes o no; utilizando el de mayor peso molecular en la capa de empuje, siendo necesario la incorporación de agentes osmóticos para acelerar la absorción de agua.20,30
Es importante contar con un balance entre los polímeros, en cuanto a la viscosidad que estos producen al momento de hidratarse, por ejemplo viscosidad muy baja en la capa de fármaco conlleva a un mal funcionamiento, provocando el desplazamiento de esta capa a los extremos, bloqueándose el orificio de salida por parte de la capa de empuje (Figura 3a). Al no tener una capa de empuje ideal y tener una mayor viscosidad en la capa del fármaco existe un desplazamiento de la capa de empuje sobre la capa del fármaco sin generar la presión osmótica requerida para que el fármaco pueda salir (Figura 3b).20,28,30,32

A partir de este sistema se han desarrollado algunas modificaciones, por ejemplo los sistemas osmóticos dirigidos al colon (OROS-CT®). El cual consiste de 5 a 6 sistemas osmóticos bicompartimentales cubiertos por un recubrimiento entérico, a través de una cápsula de gelatina dura (Figura 4). A partir de su administración, la cápsula de gelatina dura se disuelve mientas que el recubrimiento entérico cumple la función de evitar la entrada de fluidos gástricos al sistema. A medida que el sistema OROS-CT® entra en el intestino delgado, el recubrimiento entérico se disuelve y el agua se introduce en el núcleo activando los sistemas push-pull.3,16,33

Sistemas osmóticos tipo sándwich
Los comprimidos osmóticos tipo sándwich consisten en una capa de empuje en medio de dos capas de fármaco (Figura 5). Recubiertos por una membrana semipermeable y tienen dos perforaciones en cada lado del comprimido. En estos comprimidos la liberación del fármaco ocurre por los dos orificios, lo que puede reducir potencialmente la irritación local por parte del fármaco en la mucosa gástrica.11,34,35 Este sistema ha sido empleado para nifedipino en el tratamiento de la hipertensión arterial y la angina de pecho.35

Sistemas osmóticos monolíticos
Este tipo de sistemas consisten en la dispersión de un agente soluble en agua (agente osmótico) en una matriz polimérica (Figura 6). El fármaco insoluble es suspendido en la matriz y la cinética de liberación de orden cero está dada tanto por el efecto osmótico como por la capacidad del polímero de mantener el fármaco suspendido. La tableta formada es recubierta por una membrana semipermeable, sobre la que se genera el orificio de liberación. Cuando estos sistemas entran en contacto en un ambiente acuoso dicha matriz sufre rupturas liberándose a través de ellas al medio externo el principio activo. El fármaco insoluble es suspendido en la matriz y la cinética de liberación de orden cero está dada por el efecto osmótico y por la capacidad del polímero de mantener el fármaco suspendido. Sin embargo, este sistema se ve alterado en la liberación del fármaco de una forma impredecible cuando se utilizan grandes dosis puesto que el proceso de lixiviación se ve reducido.2,36,37

Bombas osmóticas con una segunda cámara no expandible
Este grupo, puede dividirse en dos subgrupos, dependiendo la función de la segunda cámara. En el primer subgrupo, la segunda cámara es usada para diluir la solución del fármaco, liberándola del dispositivo. Esto se hace porque en algunos casos, si el fármaco deja el dispositivo como una solución saturada, puede haber irritación en el tracto gastrointestinal. El segundo subgrupo consiste en dos tabletas tipo BOE en una sola tableta. Cada una de las tabletas BOE puede contener diferentes fármacos. Este dispositivo puede liberar ambos fármacos simultáneamente.1,2
Bombas osmóticas por porosidad controlada
Este tipo de bombas están basadas en las BOE. Sin embargo estas bombas se diferencian en el tipo de membrana, puesto que en ella contiene aditivos solubles en agua, los cuales después de estar en contacto en un ambiente acuoso se disuelven, resultando en una formación in situ de microporos en la membrana (Figura 7). Algunos de estos aditivos formadores de microporos usado en este tipo de sistemas son el cloruro de sodio, urea y cloruro de potasio.2,38

A partir de la incorporación de estos aditivos a la membrana, ésta es sustancialmente permeable al agua y a los solutos disueltos provocando que el mecanismo de liberación del fármaco se realice a través de difusión controlada por la presión osmótica generada desde el núcleo. La velocidad de liberación de estos sistemas depende del espesor de la membrana, del nivel de solubilidad de los componentes de la membrana, de la solubilidad del fármaco y de la presión osmótica.2,13
Sistemas multiparticulados
En estos sistemas son utilizados pellets los cuales contienen el fármaco y pueden tener o no, un agente osmótico, éstos son recubiertos con membrana pelicular regularmente de acetato de celulosa (Figura 8). Cuando entran en contacto en el ambiente acuoso, el agua penetra dentro del núcleo y forma una solución saturada de los componentes solubles. La presión osmótica induce a una afluencia de agua, que a consecuencia, resulta en una rápida expansión de la membrana con el objetivo de formar poros. El fármaco es liberado a través de estos, siguiendo una cinética de orden cero. Este tipo de sistemas está claramente influenciado por los componentes de la membrana y la adición de plastificantes.2,39,40

Sistemas osmóticos líquidos
Los sistemas osmóticos orales líquidos (L-OROS®) están formados por un compartimiento el cual contiene al fármaco disuelto, también está constituido por una membrana semipermeable, una capa osmótica y un orificio para la subsiguiente liberación del fármaco. Existen tres tipos y son: L-OROS® de gelatina blanda (Figura 9), gelatina dura, así como el sistema retardado administrado a través de un bolo.

En general, cuando el sistema entra en contacto con el medio acuoso, el agua penetra a través de la membrana semipermeable hasta activar la capa osmótica. La expansión de la capa osmótica desarrolla una presión hidrostática dentro del sistema, lo que obliga la salida del fármaco por el orificio de salida.
En el caso de los sistemas L-OROS® de gelatina blanda y dura, están diseñados principalmente para ejercer una liberación continua del fármaco, por otro lado el sistema retardado administrado a través de un bolo, está diseñado para proporcionar un impulso a la capa del fármaco. Este sistema comprende tres capas: una capa de retardo o de placebo que consiste regularmente en un polímero inerte, una capa de fármaco y una capa osmótica, todo ello rodeado por una membrana semipermeable. El orificio de salida está ubicado en este caso, en el extremo de la capa del placebo; en conjunto el dispositivo se encuentra en forma de cápsula (Figura 10).

El sistema retardado administrado a través de un bolo puede retrasar la liberación del fármaco de 1 a 10 horas, dependiendo de la permeabilidad de la membrana semipermeable y el espesor de la capa de placebo. Esto permite que el sistema se dirija hacia áreas específicas del tracto GI para la entrega del fármaco. Estos sistemas líquidos en general, están diseñados principalmente para suministrar fármacos como formulaciones líquidas combinando los beneficios de liberación prolongada con una alta biodisponibilidad.1,3,16,33,43
Patentes
En el mercado se encuentran 31 productos basados en esta tecnología y cubren principalmente 4 áreas terapéuticas: la cardiovascular (35%), neurológica (25%), enfermedades de temporada (25%) y desordenes metabólicos (15%). Existían alrededor de 240 patentes en USA de sistemas de liberación osmóticos hasta lo que fue 1993, de los cuales más del 50% eran sistemas orales, después de ese año se incremento considerablemente el número de patentes registradas. La compañía Alza Corp. es la que más ha registrado patentes de sistemas tipo oral a lo largo del tiempo, compañías como Pfizer y Merck sólo tienen algunas patentes registradas, en la tabla 3 se muestran algunas patentes. Debido a las restricciones de las patentes sólo 14 trabajos de investigación fueron publicados con respecto a aspectos de formulación contra 161 patentes registradas tan sólo en el año 2000. En estos últimos años con las patentes primarias vencidas, muchos competidores entraron en el campo, lo que subsecuentemente incrementó el número de patentes. El crecimiento en el campo de la propiedad intelectual ha creado en los últimos 10 años más de 200 publicaciones de estudios clínicos en cuanto a bioequivalencia, tolerabilidad, seguridad y eficacia de formulaciones genéricas.14

Conclusión
Los sistemas osmóticos orales han demostrado su utilidad y versatilidad en la administración de fármacos con solubilidades variables. Este tipo de sistemas podrían ayudar a optimizar los sistemas de liberación de fármacos, debido a las ventajas que presentan en comparación con los sistemas convencionales, tales como la liberación del fármaco a una velocidad predeterminada e independencia de parámetros fisiológicos. Por lo tanto este tipo de sistemas tiene un futuro potencial importante en la innovación de formulaciones convencionales y en el desarrollo mercantil, a la vez que muchas patentes están por terminar su periodo de validez, abriendo puertas para la generación de productos genéricos.
Referencias
1. Gupta S, Singh RP, Sharma R, Kalyanwat R, Lokwani P. Osmotic pumps: a review. Pharmacie Globale IJCP. 2011; 2(6):1-8. [ Links ]
2. Verma RK, Mishra B, Garg S. Osmotically controlled oral drug delivery. Dr Dev Ind Pharm. 2000; 26(7): 695-708. [ Links ]
3. Gupta R, Gupta R, Basniwal PK, Rathore GS. Osmotically controlled oral drug delivery systems: a review. Int J Ph Sci. 2009; 1(2): 269-275. [ Links ]
4. Rose S, Nelson JF. A continuous long-term injector. Australian J Exp Bio Med Sci. 1955; 33(4):415-419. [ Links ]
5. Higuchi T. Osmotic dispenser with collapsible supply container. US Patent No. 3, 760,805, 1973. [ Links ]
6. Higuchi T, Leeper HM. Improved osmotic dispenser employing magnesium sulfate and magnesium chloride. US Patent No. 3760804, 1973. [ Links ]
7. Higuchi T, Leeper HM. Osmotic dispenser with means for dispensing active agent responsive to osmotic gradient. US Patent No. 3995631, 1976. [ Links ]
8. Theeuwes F. Elementary osmotic pump. J Pharm Sci. 1975; 64 (12): 1987-1991. [ Links ]
9. Cortese R, Theeuwes F. Osmotic device with hydrogel driving member. US Patent No. 4, 327,725, 1982. [ Links ]
10. Wong PSI, Barclay B, Deters JC, Theeuwes F. Osmotic device with dual thermodynamic activity. US Patent 4612008, 1986. [ Links ]
11. Keraliya RA, Patel C, Patel P, Keraliya V, Soni TJ, Patel RC, Patel MM. Osmotic drug delivery systems a part of modified release dosage form. ISRN Pharmaceutics. 2012. doi:10.5402/2012/528079. [ Links ]
12. McClelland GA, Sutton SC, Engle K, Zentner GM. The solubility-modulated osmotic pump: in vitro/in vivo release of diltiazem hydrochloride. Pharm Res. 1991; 8(1): 88-92. [ Links ]
13. Gupta BP, Thakur N, Jain NP, Banweer J, Jain S. Osmotically Controlled Drug Delivery System with Associated Drugs. J Pharm Pharmaceutical Sci. 2010; 13(3): 571-588. [ Links ]
14. Malaterre V, Ogorka J, Loggia N, Gurny R. Oral osmotically driven systems: 30 years of development and clinical use. Eur J Pharm Biopharm. 2009; 73(3):311-23. [ Links ]
15. Shapiro M, Jarema MA, Gravina S. Magnetic resonance imaging of an oral gastrointestinal-therapeutic-system (GITS) tablet. J Control Release. 1996; 38: 123-127. [ Links ]
16. Verma RK, Krishna DM, Garg S. Formulation aspects in the development of osmotically controlled oral drug delivery systems. J Control Release. 2002; 79: 7-27. [ Links ]
17. Thombre AG, DeNoto AR, Gibbes DC. Delivery of glipizide from asymmetric membrane capsules using encapsulated excipients. J Control Release. 1999; 60: 333-341. [ Links ]
18. Theeuwes F. Osmotic dispenser with gas generating means. US patent 4,036,228, 1977. [ Links ]
19. Okimoto K, Rajewski RA, Stella VJ. Release of testosterone from an osmotic pump tablet utilizing (SBE) -7m -β- CD as both a solubilizing and an osmotic pump agent. J Control Release. 1999; 58: 29-38. [ Links ]
20. Malaterre V, Ogorka J, Loggia N, Gurny R. Evaluation of the tablet core factors influencing the release kinetics and the loadability of push-pull osmotic systems. Dr Dev IndPharm. 2008; 1:1-7. [ Links ]
21. Chen C, Lee D, Xie J. Controlled release formulation for water insoluble drugs in which a passageway is formed in situ. US patent No. 5736159, 1998. [ Links ]
22. Guittard GV, Deters JC, Theeuwes F, Cortese R. Osmotic system with instant drug availability. US patent 4,673, 405, 1987. [ Links ]
23. Seminoff LA, Zentner GM. Cellulosic coating. US patent 5,126,146, 1992. [ Links ]
24. Santus G, Baker RW. Osmotic drug delivery: A review of the patent literature. J Control Release. 1995; 35: 1-21. [ Links ]
25. Lindstedt B, Ragnarsson G, Hjartstam J. Osmotic pumping as a release mechanism for membrane-coated drug formulations. Int J Pharm. 1989; 56: 261-268. [ Links ]
26. Okimoto K, Ohike A, Ibuki R, Aoki O, Ohnishi N, Rajewsi RA. Factors affecting membrane-controlled drug release for an osmotic pump tablet (OPT) utilizing (SBE)7m-β-CD as both a solubilizer and osmotic agent. J Control Release. 1999; 60(2): 311-319. [ Links ]
27. Liu L, Khang G, Rhee JM, Lee HB. Monolithic osmotic tablet system for nifedipine delivery. J Control Release. 2000; 67: 309-322. [ Links ]
28. León G, Melgoza LM. Comprimidos osmóticos bicompartimentales. Rev. en Industria Farmacéutica. 2012; 168(1):88-93. [ Links ]
29. Theeuwes F. Oros osmotic system-development. Dr Dev Ind Pharm. 1983; 9:1331-1357. [ Links ]
30. Malaterre V, Ogorka J, Loggia N, Gurny R. Approach to design push-pull osmotic pumps. Int J Pharm. 2009; 376: 56-62. [ Links ]
31. Malaterre V, Pedersen M, Ogorka J, Gurny R, Loggia N, Taday PF. Terahertz pulsed imaging, a novel process analytical tool to investigate the coating characteristics of push-pull osmotic systems. Eur J Pharm Biopharm. 2009. doi:10.1016/j.ejpb.2008.10.011. [ Links ]
32. Thombre AG, Appel LE, Chidlaw MB, Daugherity PD, Dumont F, Evans LAF, Sutton SC. Osmotic drug delivery using swellable-core technology. J Control Release. 2004; 94: 75-89. [ Links ]
33. Ghosh T, Ghosh A. Drug delivery through osmotic systems - an overview. J App Pharm Sci. 2011; 1(2): 38-49. [ Links ]
34. Cortese R, Barclay B, Theeuwes F. Simultaneous delivery of two drugs from unit delivery device. US Patent No. 4449983, 1984. [ Links ]
35. Liu LX, Khang G, Rhee JM, Lee HB. Sandwiched osmotic tablet core for nifedipine controlled delivery. Bio Med Mat Eng. 1999; 9: 297-310. [ Links ]
36. Fassihi R, Pillay V. Monolithic tablet for controlled drug release. US 6090411, 2000. [ Links ]
37. Lu EX, Jiang ZQ, Zhang QZ, Jiang XQ. A water-insoluble drug monolithic osmotic tablet system utilizing gum arabic as an osmotic, suspending and expanding agent. J Control Release. 2003; 92: 375-382. [ Links ]
38. Haslem J, Rork GS. Controlled porosity osmotic pump. US Patent 488063, 1989. [ Links ]
39. Schultz P, Kleinebudde P. A new multiparticulate delayed release system. Part I: Dissolution properties and release mechanism. J Control Release. 1997; 47(2): 181-189. [ Links ]
40. Dey NS, Majumdar S, Rao MEB. Multiparticulate drug delivery systems for controlled release. Tropical J Pharma Res. 2008; 7(3): 1067-1075. [ Links ]
41. Cortese R, Barclay B, Theeuwes F. Osmotic device for dispensing two different medications. US Patent No. 4455143, 1984. [ Links ]
42. Zentner GN, McClelland GA, Sutton SC. Controlled porosity solubility and resin modulated Osmotic drug delivery. J Control Release. 1991; 16: 237-44. [ Links ]
43. Baena Y, Aragón M, Sandoval PA, Rosas JE, Ponce D'León LF. Sistemas osmóticos de administración oral. Rev Col Cienc Quim Farm. 2006; 35(2): 192-211. [ Links ]














