ANTECEDENTES
La mortalidad materna, como problema de salud pública, hace evidente la inequidad al acceso, disponibilidad y calidad de los servicios de salud, y es un indicador de desarrollo social. En México, la preeclampsia sigue siendo una de las principales causas de morbilidad y mortalidad materna, problema que debe enfrentarse, en la atención primaria, con prevención, detección y tratamiento oportuno. El seguimiento estrecho de la mujer embarazada,1,2 y de todas las acciones con repercusión positiva en la disminución de la morbilidad y mortalidad materna y perinatal es decisivo para mejorar la calidad de vida de la madre y del recién nacido.
La evidencia de los últimos 20 años deja en claro la necesidad del tamizaje de preeclampsia entre las 11 a 13.6 semanas, junto con la búsqueda de los diferentes marcadores biofísicos, bioquímicos y ultrasonográficos que permitan cuantificar el riesgo específico de cada paciente para afinar la predicción y poner en marcha acciones oportunas que mejoren las condiciones del embarazo y el desenlace perinatal; es necesario insistir en el cumplimiento de las consultas prenatales de rutina según el riesgo específico de cada paciente.3,4
La preeclampsia afecta, aproximadamente, a 3% de todos los embarazos1 y es causa importante de morbilidad y mortalidad materna y perinatal6 y una de las primeras causas de muerte materna en México. 7 Sobreviene cuando falla la invasión trofoblástica a las arterias espirales y se alteran la perfusión placentaria, aparece la isquemia y la disfunción endotelial después de las 20 semanas de gestación. 8 Existen pruebas clínicas que predicen eficazmente la preeclampsia entre las 11-13.6 semanas; para esto se utilizan algoritmos que combinan la historia de la madre, el índice de pulsatilidad medio de las arterias uterinas, la presión arterial media de la madre, las concentraciones séricas de la proteína plasmática A asociada al embarazo y el factor de crecimiento placentario. 9,10,11 En las pacientes con alto riesgo, el tratamiento profiláctico temprano con aspirina puede disminuir, incluso en 80%, la aparición de preeclampsia.12-15
Para la estandarización de las mediciones en el cribado del riesgo de preeclampsia se utilizan como unidad de medida los múltiplos de la mediana, que se obtienen al dividir el valor del marcador por la mediana propia para el marcador y las semanas de embarazo. La ecuación para estimación y corrección de los parámetros la publicaron Nicolaides, Sniders y Cuckle y la distribución normal multivariante Reynolds y Penney. 16 Para el marcador y las semanas de embarazo se tomaron en cuenta los siguientes parámetros: índice de pulsatilidad medio de las arterias uterinas, proteína plasmática A asociada al embarazo, factor de crecimiento placentario y presión arterial media que permite detectar el riesgo específico en pacientes embarazadas de preeclampsia, disminuyendo la morbilidad y mortalidad materna y perinatal. 17,18,19
El objetivo de este estudio fue: calcular y ajustar los múltiplos de la mediana para el índice de pulsatilidad medio de las arterias uterinas, presión arterial media materna, factor de crecimiento placentario y proteína plasmática A asociada al embarazo, a fin de valorar el desempeño diagnóstico del modelo corregido de preeclampsia de la Fetal Medicine Foundation en población mexicana.
MATERIALES Y MÉTODOS
Estudio de casos y controles anidado en una cohorte prospectiva efectuado en el Centro de Salud Dr. Galo Soberón y Parra, Jurisdicción Sanitaria Azcapotzalco de los Servicios de Salud Pública de la Ciudad de México, entre el 1 de octubre de 2015 y el 30 de junio de 2016. Todas las pacientes autorizaron y firmaron el consentimiento informado antes de incorporarlas al protocolo de estudio. Criterios de inclusión: pacientes de riesgo no seleccionado, con embarazo único, entre 11 y 13.6 semanas calculadas por ecografía mediante longitud cráneo cauda. Criterio de exclusión: pacientes con más de 14 semanas de embarazo, gestación múltiple, ingesta de medicamentos antes del embarazo (antihipertensivos, antitiroideos, insulina, diuréticos). Criterio de eliminación: pacientes que abandonaron el estudio.
La muestra se calculó en relación con la cantidad de pacientes que acudieron a ultrasonido entre las 11-13.6 semanas de embarazo en el año 2014 al servicio de Medicina materno fetal del Centro de Salud Dr. Galo Soberón y Parra, y fueron 1367. Se utilizaron índice de confianza de 95%, margen de error del 5% y probabilidad de ocurrencia y no ocurrencia de 50% en relación con preeclampsia:
Se integró la historia clínica de todas las pacientes para identificar los factores de riesgo. La presión arterial se tomó en dos ocasiones, en cada brazo, con un baumanómetro digital y somatometría (talla y peso). Las mediciones ultrasonográficas (longitud cráneo cauda e IPm AUt) se tomaron con un equipo Voluson (GE USA), mediante ecografía abdominal con la metodología aprobada por la Fetal Medicine Foundation con el feto en posición neutra, en un corte sagital medio como medida mínima 45 mm y máxima 84 mm.
Con la paciente en ayuno de más de 4 horas se tomaron 5 mL de sangre materna, se separó el paquete globular del suero mediante centrifugación y, posteriormente, se refrigeró hasta el análisis final. Para determinar las concentraciones del factor de crecimiento placentario y proteína plasmática A asociada al embarazo se utilizó la plataforma de acceso clínico aleatorio DelfiaXpress (PerkinElmer Human and analitycal sciences Whaltham Mass and Turku Finland). Ninguna muestra se congeló y descongeló más de una ocasión.
Se utilizó estadística descriptiva e inferencial. La distribución de las variables se realizó mediante la prueba de Kolmogorov-Smirnoff. Las variables normalmente distribuidas se analizaron con t de Student y se expresaron como media y desviación estándar, las variables con distribución libre se analizaron con U de Mann-Whitney y se expresaron como mediana y rango intercuartil (RIQ) o rango mínimo y máximo (rango).
Los biomarcadores se transformaron a su valor logarítmico. Los múltiplos de la mediana se calcularon como la diferencia del valor logarítmico observado de cada biomarcador, con el valor esperado de acuerdo con las distintas fórmulas para cada biomarcador, según la Fetal Medicine Foundation. Se comparó la distribución entre los valores observados en población mexicana, con los valores esperados según la fórmula original de la Fetal Medicine Foundation. Cuando la diferencia fue mayor a 0.2 múltiplos de la mediana, se hizo el ajuste de la fórmula del valor esperado al agregar el valor de la mediana del observado de cada biomarcador como coeficiente de efectos fijos y multiplicado por 10 potenciado a la fórmula original. El desempeño del modelo ajustado se realizó mediante el cálculo de sensibilidad (Se), tasa de falsos positivos (Sp) y área bajo la curva. El programa de cómputo utilizado fue Spotfire S+ 8.1 versión 3.4 TIBCO Software Inc. Para el análisis de múltiplos de la mediana se utilizó el programa SAS analytics; y para determinar el riesgo de padecer preeclampsia en cada paciente se utilizó el programa de la Fetal Medicine Foundation (www.fetalmedicine.org) basado en el algoritmo de cálculo propuesto por Cuckle y Nicolaides y estandarizado con el número de patente WO2012076553A2.
RESULTADOS
De las 300 pacientes, 3 abandonaron el estudio por cambio de adscripción en el Sector Salud y 5 más se eliminaron por cambio de residencia; quedaron 292 pacientes. La media de edad de las madres fue de 23 años (límites 14 y 40) (Cuadro 1). La media de semanas de embarazo al momento del tamizaje fue de 12.4 (DE ± 0.72). La media de peso fue de 61.9 kg (rango 34.8-107) (Cuadro 2). Se obtuvo la distribución de cada marcador y los resultados se normalizaron a valores múltiplos de la mediana, se aplicó la ecuación de tercer grado acorde con los diferentes factores: peso, tabaquismo y etnia.
Cuadro 1 Distribución de la edad materna según las semanas de embarazo al momento del tamizaje
| Semanas | n | Media | DE | Min | Max |
| 11 | 65 | 21.0 | 5.44 | 15.0 | 36.0 |
| 12 | 115 | 24.0 | 5.66 | 14.0 | 40.0 |
| 13 | 112 | 24.0 | 5.66 | 15.0 | 39.0 |
| Total | 292 | 23.0 | 5.68 | 14.0 | 40.0 |
Cuadro 2 Complicaciones fetales en diabetes gestacional
| Semanas | n | Media | DE | Min | Max |
| 11 | 65 | 57.7 | 13.18 | 38.7 | 91.1 |
| 12 | 115 | 61.0 | 14.86 | 34.8 | 105.1 |
| 13 | 112 | 65.0 | 13.93 | 40.0 | 107.0 |
| Total | 292 | 61.9 | 14.19 | 34.8 | 107.0 |
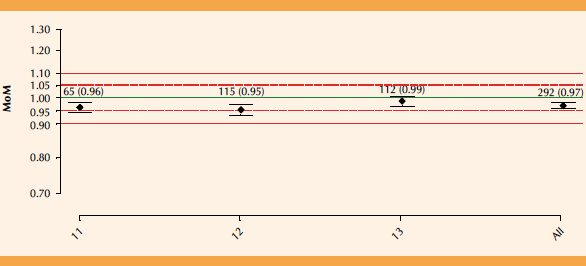
La media del múltiplo de la mediana del IP medio de las arterias uterinas fue de 1.24; por eso se efectuó el siguiente ajuste: UtPI = 1.24 (2.6922-0.01455 x las semanas de embarazo) (Figura 1). La proteína plasmática A asociada al embarazo requirió un ajuste de 0.80 en la fórmula predeterminada PlGF = 0.80 x 10^ (3.67452 - 0.0655563 (semanas de embarazo) + 0.000455729 x semanas de embarazo ^2) (Figura 2). La proteína plasmática A asociada al embarazo requirió un ajuste de 0.81 en la ecuación predeterminada PAPP-A = 0.81 x 10^ (-0.41242+0.0611984 x las semanas de embarazo -0.000200483 x las semanas de embarazo ^2) (Figura 3). En relación con la proteína plasmática A asociada al embarazo no existió sesgo ni se requirió ajuste de la ecuación predeterminada. Figura 4

Figura 1 Distribución de múltiplos de la mediana original y ajustada del índice de pulsatilidad medio de las arterias uterinas.

Figura 2 Distribución de múltiplos de la mediana original y ajustado del factor de crecimiento placentario.

Figura 3 Distribución de múltiplos de la mediana originales y ajustados de proteína plasmática asociada al embarazo.
Las 292 pacientes tuvieron seguimiento hasta la finalización del embarazo. Con el modelo ajustado, 9.5% (28/292) de las pacientes se clasificaron con alto riesgo de preeclampsia, con prevalencia de la enfermedad de 4.5% (13/292). En el Cuadro 3 está la cantidad de pacientes con preeclampsia conforme a las semanas de embarazo en que se practicó el tamizaje y se estableció el diagnóstico. La sensibilidad, falsos positivos y área bajo la curva del modelo ajustado para detectar cualquier preeclampsia fue de 92% (12/13), 5.7% (16/279) y 93.3%, respectivamente. Para las 10 pacientes con preeclampsia antes de las 37 semanas, la sensibilidad, falsos positivos y área bajo la curva fue de 100% (10/10), 6.4% (18/282) y 96.8%, respectivamente; mientras que de las 3 pacientes con preeclampsia posterior a la semana 37, la sensibilidad, falsos positivos y área bajo la curva fue de 66.7% (2/3), 10% (26/289) y 78.8%, respectivamente. Cuadro 4
Cuadro 3 Casos que resultaron con preeclampsia según las semanas de embarazo al tamizaje y diagnóstico de la complicación
| Caso | Semanas al tamizaje | Semanas al diagnóstico de preeclampsia |
| 1 | 11.4 | 34.1 |
| 2 | 12.6 | 35.3 |
| 3 | 12.4 | 28.1 |
| 4 | 13.2 | 32.0 |
| 5 | 11.3 | 31.5 |
| 6 | 12.2 | 32.6 |
| 7 | 13.0 | 37.4 |
| 8 | 12.5 | 34.2 |
| 9 | 11.6 | 33.6 |
| 10 | 13.1 | 37.6 |
| 11 | 11.5 | 34.1 |
| 12 | 13.6 | 39.1 |
| 13 | 11.3 | 35.1 |
DISCUSIÓN
La correlación del tamizaje practicado para detectar preeclampsia en este estudio incluyó factores de riesgo de la madre, presión arterial media materna, índice de pulsatilidad medio de las arterias uterinas mediante flujometría Doppler, determinación de las concentraciones en suero materno del factor de crecimiento placentario y proteína plasmática A asociada al embarazo, con la metodología propuesta por Nicolaides. 20 La primera diferencia es que se efectuó en el primer nivel de atención médica de los Servicios de Salud Pública de la Ciudad de México, en población mexicana no seleccionada, lo que permitió clasificar oportunamente a las embarazadas en bajo o alto riesgo de preeclampsia, con el mismo algoritmo de la Fetal Medicine Foundation.
Los resultados obtenidos en relación con el índice de pulsatilidad de las arterias uterinas difieren de los reportados por otras investigaciones. El índice de pulsatilidad más alto fue de 2.93 vs 2.35 en Inglaterra por Nicolaides y su grupo. 9 Esta diferencia puede explicarse por las características de las madres existentes en cada población; fue necesario ajustar la ecuación del esperado por 1.24.
Los marcadores bioquímicos confirman lo descrito por Poon, Nicolaides y colaboradores en pacientes con alto riesgo de preeclampsia. Los valores fueron 20% más bajos para el factor de crecimiento placentario y para la proteína plasmática A asociada al embarazo.18,19,20 Las concentraciones séricas entre las 11 a 13.6 semanas fueron significativamente más bajas en las pacientes con preeclampsia con 0.824 múltiplos de la mediana para factor de crecimiento placentario y 0.748 múltiplos de la mediana para proteína plasmática A asociada al embarazo. 21 Está demostrado que la población mexicana es bioquímicamente diferente de la población europea y que se requieren ajustes locales y periódicos para cada centro o laboratorio. 22 Los resultados del cálculo de múltiplos de la mediana en población mexicana fueron aún más bajos para las pacientes con preeclampsia de 0.77 múltiplos de la mediana para factor de crecimiento placentario y 0.73 múltiplos de la mediana para proteína plasmática A asociada al embarazo.
La principal limitación de este estudio fue el tamaño de la muestra utilizado para calcular los múltiplos de la mediana, circunstancia que puede limitar su validación externa. El objetivo de este estudio fue: explorar el ajuste de las fórmulas originales y valorar el desempeño diagnóstico de un modelo ajustado a población mexicana que diera pie a futuras investigaciones con una muestra representativa de la población general. Las fortalezas del estudio radican en el seguimiento de los lineamientos de la Fetal Medicine Foundation para el análisis de cada marcador y para el ajuste de medianas, que son procesos estandarizados y reconocidos internacionalmente, por lo que los factores de corrección obtenidos en este estudio son sólidos y confiables.
CONCLUSIONES
La distribución de los múltiplos de la mediana en población mexicana es distinta para los biomarcadores: factor de crecimiento placentario, proteína plasmática A asociada al embarazo e índice de pulsatilidad medio de las arterias uterinas, su ajuste a la población estudiada permitió determinar la tasa de detección adecuada de preeclampsia. Este estudio puede dar pie a futuras investigaciones con mayor cantidad de pacientes que permita el ajuste de cada biomarcador para la población mexicana; con esto se conseguirá mejorar el desempeño diagnóstico del modelo de preeclampsia de la Fetal Medicine Foundation a nuestra población.











 nueva página del texto (beta)
nueva página del texto (beta)